题目内容
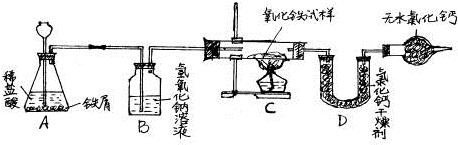
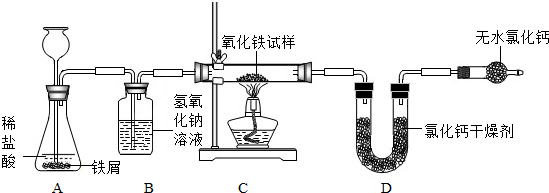
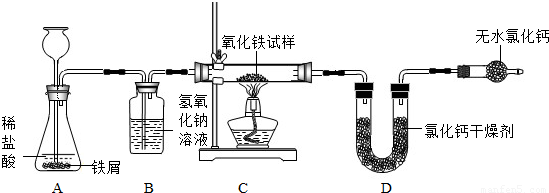
某化学探究活动小组的小峰同学为了测定某不纯氧化铁试样(其中的杂质不参与反应)中氧化铁的质量分数,设计了如下图所示的实验装置.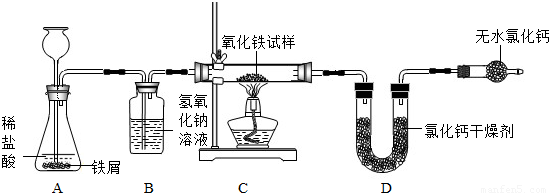
试回答下列问题:
(1)写出A中发生反应的化学方程式:______.
(2)小峰同学通过称量反应前、后D部分的质量,来计算试样中氧化铁的质量分数,若按这一方案进行实验并记录数据,则计算出的结果和实际值相比将______(填“偏大”、“偏小”或“相同”).
(3)对于小峰同学设计的这个实验方案,谈谈你的评价意见和建议.
【答案】分析:(1)铁与盐酸反应生成氯化亚铁和氢气,可以写出化学方程式;
(2)反应装置A和B会带出一部分水蒸气,会被D装置吸收,而使水的实际质量增加,可以据此答题;
(3)根据装置的特点可以知道,产生的气体通过装置B时会带出水蒸气,而影响实验结果.
解答:解:(1)可以直接写出化学方程式;
(2)反应装置A和B会带出一部分水蒸气,会被D装置吸收,而使水的实际质量增加,所以若根据质量差进行计算则会使计算结果偏大;
(3)为了使实验结果更准确,应该在B和C之间加一个干燥装置;
故答案为:(1)Fe+2HCl═FeCl2+H2↑;
(2)偏大;
(3)不正确,应在B和C之间加一个浓硫酸吸水装置.
点评:本题主要考查氢气还原氧化铁、书写化学方程式等方面的知识,书写化学方程式时要注意遵循质量守恒定律.
(2)反应装置A和B会带出一部分水蒸气,会被D装置吸收,而使水的实际质量增加,可以据此答题;
(3)根据装置的特点可以知道,产生的气体通过装置B时会带出水蒸气,而影响实验结果.
解答:解:(1)可以直接写出化学方程式;
(2)反应装置A和B会带出一部分水蒸气,会被D装置吸收,而使水的实际质量增加,所以若根据质量差进行计算则会使计算结果偏大;
(3)为了使实验结果更准确,应该在B和C之间加一个干燥装置;
故答案为:(1)Fe+2HCl═FeCl2+H2↑;
(2)偏大;
(3)不正确,应在B和C之间加一个浓硫酸吸水装置.
点评:本题主要考查氢气还原氧化铁、书写化学方程式等方面的知识,书写化学方程式时要注意遵循质量守恒定律.

练习册系列答案
相关题目
某化学探究活动小组的小峰同学为了测定某不纯氧化铁试样(其中的杂质不参与反应)中氧化铁的质量分数,设计了如图所示的实验装置.(注:3H2+Fe2O3 2Fe+3H2O)
2Fe+3H2O)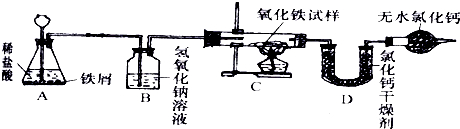
试回答下列问题:
(1)写出A中发生反应的化学方程式:______.
(2)若已知C中玻璃管的质量为100g,并称量了以下相关数据:
| 质量g | 反应前 | 反应后 |
| ①C中玻璃管与样品质量 | 120g | 115.2g |
| ②D中U型管与干燥剂质量 | 200g | 206g |