题目内容
【题目】某同学利用下图装置验证二氧化碳的相关化学性质。
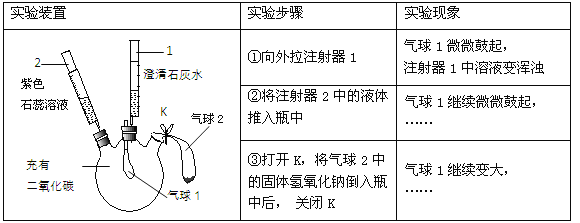
(1)步骤①中发生反应的化学方程式是 。
(2)补全步骤②中的现象: 。
(3)补全步骤③中的现象: ,其中“气球1继续变大”的原因是 。
(4)通过本实验能验证的二氧化碳的化学性质是_____。
【答案】(1)Ca(OH)2 + CO2=CaCO3↓+ H2O ;(2)紫色石蕊溶液变红;
(3)溶液由红色变为蓝色 二氧化碳与氢氧化钠反应使容器内气体减少,压强减小;
(4)二氧化碳分别能与氢氧化钙、氢氧化钠反应。
【解析】
试题分析:⑴①向外拉注射器1,使容器内的压强减少,容器内的二氧化碳进入注射器,与氢氧化钙反应生成碳酸钙沉淀和水;⑵②二氧化碳与水反应生成碳酸,使溶液显酸性,紫色石蕊试液变红色,容器内的压强继续减少,气球1继续胀大;⑶③氢氧化钠与二氧化碳反应,使容器内的压强继续减少,使气球1继续胀大;⑷由以上探究可以得出:二氧化碳分别能与氢氧化钙、水和氢氧化钠反应。

 中考解读考点精练系列答案
中考解读考点精练系列答案【题目】FeCl3可用作催化剂和外伤止血剂.某实验兴趣小组利用FeCl3腐蚀电路铜板后的溶液(主要成分为FeCl2、CuCl2)进行了氯化铁回收实验.
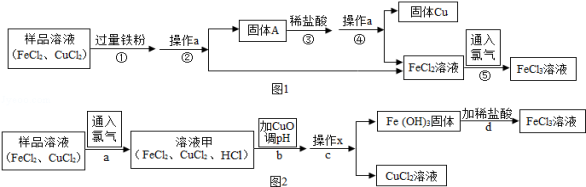
实验一:(如图1)
(1)写出步骤①中发生的化学方程式 ,此反应的基本类型是 .
(2)步骤②中的操作a名称是 ;步骤③中加入稀盐酸的目的是 .
实验二:该实验小组同学通过查阅资料,又进行了另一种尝试.
【阅读资料】不同金属氢氧化物可以在不同的pH范围内从溶液中沉淀析出,工业上利用调节溶液pH的方法,使金属氢氧化物依次沉淀,结合过滤等操作,进行物质分离.
如表是氢氧化铁与氢氧化铜开始沉淀与沉淀完全的pH
Fe(OH)3 | Cu(OH)2 | |
开始沉淀的pH | 1.9 | 4.7 |
沉淀完全的pH | 3.2 | 6.7 |
(3)如图2,步骤b加入CuO消耗溶液甲中的HCl,使溶液pH增大到所需范围,请写出盐酸与氧化铜反应的化学方程式 ;你认为步骤b调节溶液的pH到 (数值范围)比较合适.
(4)该实验需要用pH试纸测量溶液的pH,请将pH试纸的使用方法补充完整: , ,把试纸显示的颜色与标准比色卡比较,读出该溶液的pH.
(5)FeCl3溶液容易生成Fe(OH)3发生变质,在保存FeCl3溶液时,常向FeCl3溶液中加入某种酸,以防止FeCl3溶液变质,你认为选用 (用字母表示)最合理.
A.稀硝酸 B.稀硫酸 C.稀盐酸 D.稀醋酸.