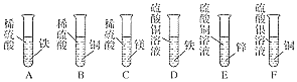
题目内容
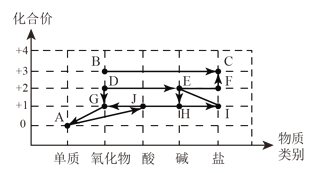
【题目】利用坐标系建立物质间的关系是总结化学知识的一种方法,A~J是初中化学常 见的十种物质,如图是根据这十种物质的类别和其中某种元素的化合价构建的它们之间的转化关系(图中“﹣”表示两端的物质间能发生化学反应,“→”表示物质间存在转化关系)。已 知农业上可用E和F等配制成具有杀菌作用的波尔多液。
(1)D的化学式是___;
(2)写出G→A反应的化学方程式___;
(3)写出F→C反应的化学方程式___;
(4)A~H八种物质能与 J 溶液反应的物质有___种。
【答案】CaO 2H2O![]() 2H2↑+O2↑ 2Al+3CuSO4=====Al2(SO4)3+3Cu 4
2H2↑+O2↑ 2Al+3CuSO4=====Al2(SO4)3+3Cu 4
【解析】
农业上可用E和F等配制成具有杀菌作用的波尔多液,E和F是氢氧化钙和硫酸铜中的一种,D为的氧化物,其中一种元素的化合价为+2价,D能转化为E,氧化钙与水反应生成氢氧化钙,则D可能是氧化钙,E为氢氧化钙,F为硫酸铜;G为氧化物,其中一种元素的化合价为+1价,D能转化为G,氧化钙与盐酸反应生成氯化钙和水,水为氧化物,氢元素的化合价为+1价,所以G为水;A的化合价0,A为单质,G(水)能转化为A,水通电分解生成氢气和氧气,A为氢气和氧气中的一种,J为酸,其中一种元素的化合价为+1价,A能转化为J,氢气在氯气中燃烧生成氯化氢,氯化氢溶于水形成盐酸,盐酸中的氢元素显+1价,所以A为氢气,J为盐酸;C为盐,其中一种元素的化合价为+3价,F(硫酸铜)能转化为C,铝与硫酸铜反应生成硫酸铝和铜,硫酸铝中的铝元素显+3价,C为硫酸铝;B为氧化物,其中一种元素的化合价为+3价,B能转化为C(硫酸铝),氧化铝与硫酸反应生成硫酸铝和水,氧化铝中的铝元素显+3价,所以B为氧化铝;H为碱,其中一种元素的化合价为+1价,H可能为氢氧化钠;I是盐,其中一种元素的化合价为+1价,E(氢氧化钙)能与I反应,氢氧化钙与碳酸钠反应生成氢氧化钠和碳酸钙,碳酸钠中的钠元素显+1价,所以I可能是碳酸钠,将猜想代入原题中,猜想成立。
根据以上分析可知:
(1)D是氧化钙,化学式是CaO;
(2)G→A的反应是水通电分解生成氢气和氧气,反应的化学方程式为:2H2O![]() 2H2↑+O2↑;
2H2↑+O2↑;
(3)F→C的反应是铝与硫酸铜反应生成硫酸铝和铜,化学方程式为:2Al+3CuSO4=====Al2(SO4)3+3Cu;
(4)A~H八种物质能与J溶液反应的物质有Al2O3、CaO、Ca(OH)2、NaOH,共4种。

【题目】同学们在课外学习活动中知道了钠和镁着火不能用CO2来灭火。他们通过查阅资料发现Mg能在CO2中燃烧:2Mg+CO2![]() 2MgO+C,但没有找到有关钠能否与CO2反应的介绍.有同学认为钠能发生类似于CO2与镁的反应,可能的化学方程式为_______________。
2MgO+C,但没有找到有关钠能否与CO2反应的介绍.有同学认为钠能发生类似于CO2与镁的反应,可能的化学方程式为_______________。
于是同学们展开了以下探究:
[实验]将燃着的钠伸入装有干燥的CO2的集气瓶中,钠能在CO2中继续燃烧。
[查阅资料]Na2O是白色固体,能与CO2反应生成Na2CO3,与H2O反应生成NaOH。
[提出猜想]同学们认为钠在CO2中燃烧的产物应该与Mg在CO2中燃烧的产物情况有所不同,并对产物提出了以下凡种猜想:通过理论分析,猜想________(填序号)肯定是错误的,理由是:______________________________________。
[验证猜想]①Na2O、C ②________、C ③NaOH、C ④Na2O、Na2CO3、C
通过理论分析,猜想________(填序号)肯定是错误的,理由是:__________________。
[验证猜想]
步骤 | 实验操作 | 主要实验现象 | 结论(燃烧产物判断) |
(1) | 将产物溶于适量水中 | 部分溶解,试管底部有黑色固体 | 燃烧产物中肯定有___ |
(2) | 取(1)所得少量上层清液,加入过量的BaCl2溶液 | _________________ | 燃烧产物中肯定有Na2CO3 |
(2) | 取(2)所得少量上层清液,加入_____溶液 | 溶液变成红色 | 燃烧产物中肯定有___ |
在步骤(2)中BaCl2溶液加入至过量的目的是____________________________________。
在步骤(3)中也可以通过加入的________方法进行检验(任写一种试剂)
[结论]猜想________(填序号)正确。