题目内容
【题目】在“宏观﹣微观﹣符号”之间建立联系,是化学学科特有的思维方式, 能帮助我们更好地认识物质变化的本质。请完成下列问题:
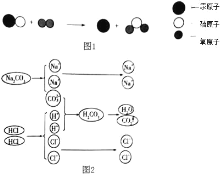
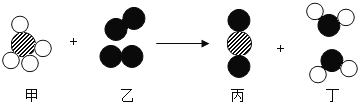
(1)晋代葛洪所著《抱朴子》一书中记载有“丹砂烧之成水银”,丹砂指的是 HgS.该反应的微观示意图可以表示为(如图1所示),请写出该反应的化学方程式_____________,微粒“ ![]() ”表示的物质属于______________(填“单质”或“化合物”)。
”表示的物质属于______________(填“单质”或“化合物”)。
(2)由初中学习可知:中和反应的微观实质是氢离子和氢氧根离子结合生成了水分子,即:H++OH-=H2O。像这种用实际参加反应的离子符号来表示化学反应的式子叫离子方程式。离子方程式的书写一般按以下步骤(以氯化镁溶液与氢氧化钾溶液反应为例):
I.写出氯化镁溶液与氢氧化钾溶液反应的化学方程式:_____________________;
Ⅱ.把易溶于水、易电离的物质写成离子形式,难溶的物质、气体和水等仍用化学式表示。上述方程式可改写成:Mg2++2C1﹣+2K++2OH﹣=Mg(OH)2↓+2C1﹣+2K+;
Ⅲ.删去两边不参加反应的离子,得离子方程式:Mg2++2OH﹣=Mg(OH)2↓。
据此回答下列问题:
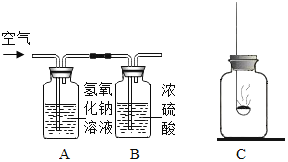
①图2 是碳酸钠溶液和稀盐酸反应的微观示意图,请写出该反应的离子方程式:____________;
②写出一个与 Zn+Fe2+=Zn2++ Fe 相对应的化学方程式___________。
③下列离子能在 pH=10 的无色溶液中共存的是________________(填序号)。
A Fe3+、Mg2+、Cl﹣、SO42- B K+、Na+、SO42- 、NO3-
C Na+、NH4+、NO3-、Cl- D H+、Cl-、K+、NO3-
【答案】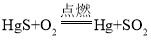 单质
单质 ![]()
![]()
![]() B
B
【解析】
(1)由图可知,该反应的化学方程式为: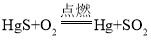 ;
;
![]() 表示的物质是由同种元素(氧元素)组成的纯净物,属于单质;
表示的物质是由同种元素(氧元素)组成的纯净物,属于单质;
(2)Ⅰ、氯化镁与氢氧化钾反应生成氢氧化镁和氯化钾,该反应的化学方程式为:![]() ;
;
①碳酸钠和稀盐酸反应生成氯化钠、二氧化碳和水,该反应的化学方程式为:![]() ,把易溶于水、易电离的物质写成离子形式,难溶的物质、气体和水等仍用化学式表示,可表示为:
,把易溶于水、易电离的物质写成离子形式,难溶的物质、气体和水等仍用化学式表示,可表示为:![]() ,删去两边不参加反应的离子,得离子方程式:
,删去两边不参加反应的离子,得离子方程式:![]() ;
;
②锌与硫酸亚铁反应生成硫酸锌和铁,该反应的化学方程式为:![]() ,删去两边不参与反应的离子,可得离子方程式为:
,删去两边不参与反应的离子,可得离子方程式为:![]() ,故填:
,故填:![]() ;
;
③A、pH=10,大于7,说明溶液显碱性,溶液中存在大量的OH-,铁离子能与氢氧根离子结合生成氢氧化铁红褐色沉淀,镁离子能与氢氧根离子结合生成氢氧化镁白色沉淀,且铁离子为黄色,不符合题意;
B、pH=10,大于7,说明溶液显碱性,溶液中存在大量的OH- ,K+、Na+、SO42-、NO3-、OH-不能形成沉淀、气体和水,可以大量共存,符合题意;
C、pH=10,大于7,说明溶液显碱性,溶液中存在大量的OH-,铵根离子能与氢氧根离子结合生成氨气,不能大量共存,不符合题意;
D、pH=10,大于7,说明溶液显碱性,溶液中存在大量的OH-,氢离子能与氢氧根离子结合生成水,不能大量共存,不符合题意。
故选B。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
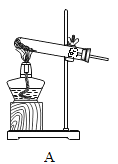
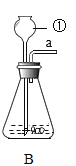
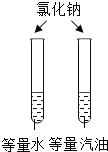
小学生10分钟应用题系列答案【题目】设计对比实验,控制变量是学习化学的重要方法,下列对比实验不能达到目的的是
编号 | ① | ② | ③ | ④ |
实验设计 |
|
|
|
|
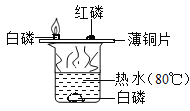
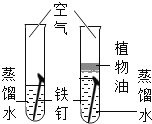
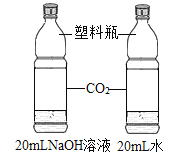
实验目的 | 探究同种物质在不同溶剂中的溶解性 | 探究可燃物燃烧的条件 | 探究铁生锈的条件 | 探究CO2与NaOH溶液能否发生反应 |
A.AB.BC.CD.D