题目内容
有一种石灰石样品,其中含有的杂质是二氧化硅(一种不溶于水,不与盐酸反应,耐高温的固体).某学生想测定该样品的纯度,他取用2克这种石灰石样品,把20克稀盐酸分4次加入,充分反应后剩余固体的质量见下表.
问:(1)2克石灰石样品中,有杂质多少克?
(2)石灰石样品的纯度是多少?
| 稀盐酸的用量 | 第1次加入5克 | 第2次加入5克 | 第3次加入5克 | 第4次加入5克 |
| 剩余固体的质量 | 1.315克 | 0.63克 | 0.3克 | 0.3克 |
(2)石灰石样品的纯度是多少?
考点:根据化学反应方程式的计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:(1)由图表分析知每加入5g盐酸会消耗0.685g固体,分析知第三次加入稀盐酸时碳酸钙已无剩余,故固体中的杂质是0.3g;
(2)利用这一量可求碳酸钙的质量分数.
(2)利用这一量可求碳酸钙的质量分数.
解答:解:
(1)由图表分析知每加入5g盐酸会消耗0.685g固体,分析知第三次加入稀盐酸时碳酸钙已无剩余,故杂质的质量为0.3g;
(2)由图表分析知第三次剩余的固体即为杂质的量,故有:
石灰石中碳酸钙的纯度为:
×100%=85%
答案:
(1)2克石灰石样品中,有杂质0.3克;
(2)石灰石样品的纯度是85%.
(1)由图表分析知每加入5g盐酸会消耗0.685g固体,分析知第三次加入稀盐酸时碳酸钙已无剩余,故杂质的质量为0.3g;
(2)由图表分析知第三次剩余的固体即为杂质的量,故有:
石灰石中碳酸钙的纯度为:
| 2g-0.3g |
| 2g |
答案:
(1)2克石灰石样品中,有杂质0.3克;
(2)石灰石样品的纯度是85%.
点评:此题是考查学生对图表的分析能力,并利用分析结果进行计算,关键是把握住完全反应的数据,利用有用的数据进行计算.

练习册系列答案
相关题目
下列能源收于可再生能源的是( )
| A、煤 | B、石油 | C、氢气 | D、天然气 |
小东同学对部分物质的性质和用途归纳如下,其中正确的是( )
A、 稀有气体填充食品袋防腐 |
B、 氧气用于气焊 |
C、 氮气通电制霓虹灯 |
D、 氧气用于光合作用 |
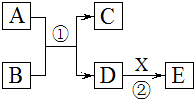 初中常见物质A、B、C、D、E、X的相互转化关系见如图.已知C是相对分子质量最小的氧化物,X的相对分子质量小于50,B是红色粉末.
初中常见物质A、B、C、D、E、X的相互转化关系见如图.已知C是相对分子质量最小的氧化物,X的相对分子质量小于50,B是红色粉末.