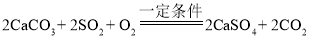题目内容
【题目】图中A、B、C分别表示三种不同的固体物质(不含结晶水),其溶解度曲线如图1所示。请回答下列问题:
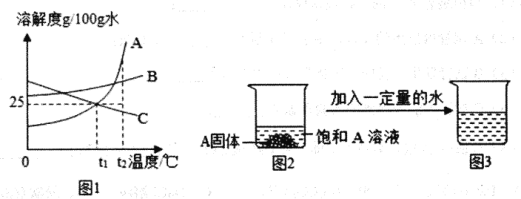
(1) t1°C时,100g水中最多溶解固体A_____________g.t2°C时,三种固体物质溶解度由小到大的顺序是_____________。写出一种将固体B的不饱和溶液转化为饱和溶液的方法____________________。
(2)t1°C时,将30g固体C加到50g水中,充分搅拌后所得溶液的质量为_________g.
(3) t2°C时分别将A、B、C的饱和溶液的降温到t1°C,其质量分数由小到大的顺序是_________________。
(4)某化学小组欲从含有少量B的A样品中,提纯A固体。可采用的提纯方法是________________(填“降温结晶”或“蒸发结晶”)。
【答案】25 C<B<A 继续加B至饱和(降温或蒸发溶剂) 62.5 C<A<B 降温结晶
【解析】
(1)由图可知t1°C时A溶解度是25g,故100g水中最多溶解固体A25g,由图可知t2°C时,三种固体物质溶解度由小到大的顺序是C<B<A,固体B的溶解度随温度升高而增大,不饱和溶液转化为饱和溶液可以继续加B至饱和(降温或蒸发溶剂),故填:25;C<B<A;继续加B至饱和(降温或蒸发溶剂)。
(2)由图可知t1°C时C溶解度是25g,30g固体C加到50g水中只能溶解12.5g,故溶液质量为50g+12.5g=62.5g,故填:62.5。
(3)t2°C时分别将A、B、C的饱和溶液的降温到t1°C,AB溶解度减小,溶质结晶析出还是饱和溶液,t1°CB溶解度大于A,故溶质质量分数B大于A,降低温度C溶解度变大,变为不饱和溶液,溶质质量分数不变,等于降温之前溶质质量分数,降温之前C溶解度,小于降温之后A溶解度,故C溶质质量分数小于A,故其质量分数由小到大的顺序是C<A<B,故填:C<A<B。
(4)提纯A固体,A溶解度岁温度升高,变化较大,可采用的提纯方法是降温结晶,故填:降温结晶。

【题目】下列实验设计能达到目的的是
选项 | A | B | C | D |
实验设计 |
|
|
|
|
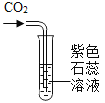
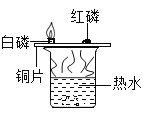
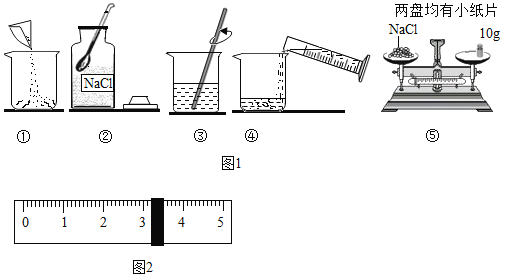
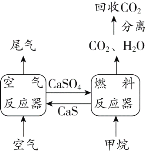
实验目的 | 证明二氧化碳与水反应生成碳酸 | 证明二氧化碳不可燃、不助燃、密度大于空气 | 证明铁铜银的活动性顺序 | 证明可燃物燃烧需要氧气和温度达到着火点 |
A.AB.BC.CD.D
【题目】实验室有一瓶在空气中露置的氢氧化钠固体样品,某兴趣小组的同学对该样品的成分及含量进行了探究。
(提出问题1)该样品中含有哪些物质?
(提出猜想)通过分析,提出如下猜想:
猜想Ⅰ:该样品中只含Na2CO3;
猜想Ⅱ:该样品中含有NaOH和Na2CO3;
猜想Ⅲ:__________________。
则NaOH变质原因的化学方程式为__________________。
(查阅资料)
①碱性的Na2CO3溶液可以与中性的CaCl2溶液发生复分解反应;
②CO2在饱和的碳酸氢钠溶液中几乎不溶解。
(实验探究1)
为确定该样品的成分,小明设计了如下实验方案,请你一起完成下列实验报告。
实验操作 | 实验现象 | 实验结论 |
(1)取少量样品溶于水,加入足量 CaCl2溶液 | ______________ | 证明猜想Ⅲ不成立;该反应的化学方程式为__________ |
(2)将上述反应后的混合液过滤,取滤液加入____________; | 溶液变红 | 证明猜想Ⅱ成立 |
(实验反思)
要除去NaOH中的Na2CO3应选择的化学试剂是_____________。
(提出问题2)如何测量该部分变质样品中碳酸钠的质量分数?
(实验探究2)
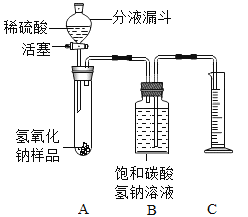
小红同学设计如图所示的装置(铁架台略去),实验在27℃,101kPa 下进行,步骤如下:
①按图连接好装置;
②用托盘天平准确称取该样品2g,放入A中试管内,向B中集气瓶中倒入饱和的碳酸氢钠溶液至瓶颈处;
③向分液漏斗中加入稀硫酸,打开活塞,让稀硫酸滴入试管中至过量,关闭活塞。反应结束后,量筒中收集到饱和的碳酸氢钠溶液244mL。
请回答下列问题:
(1)在实验步骤①和②之间,还缺少一实验步骤,该实验步骤是_______________;
(2)B中集气瓶盛装的饱和的碳酸氢钠溶液不能用水代替,其理由是_______________;
(3)试管中原有的空气对实验结果是否有明显影响?______________(填“有”或“没有”)。
(4)变质氢氧化钠样品中碳酸钠的质量分数为________________。(在27℃,101kPa时二氧化碳的密度为1.8g/L)(计算结果精确至1%)
【题目】酸、碱、盐的溶解性表是学习化学的重要工具之一。下表是部分酸、碱、盐在水中的溶解性(20。C),请回答下列问题。
阴离子 阳离子 | OH- | NO3- | CO32- | Cl- |
K+ | 溶 | 溶 | 溶 | 溶 |
Ba2+ | 溶 | 溶 | 不 | 溶 |
Cu2+ | 不 | 溶 | 不 | 溶 |
(1)上述阴、阳离子形成不溶性碱的化学式为________, 形成复合肥料的化学式为_____ 。
(2)KOH溶液和Ba(NO3)2溶液_______(填“能“或“不能“)反应,理由是_______。
(3)下列各组离子在水溶液中能大量共存的是_______________ 。
A. OH-H+Ba2+NO![]() B. OH-Ba2+K+Cl-
B. OH-Ba2+K+Cl-
C. CO![]() K+Ba2+Cl-D. CO
K+Ba2+Cl-D. CO![]() Cu2+NO
Cu2+NO![]() K+
K+