题目内容
经测定某生石灰样品中含有25%的碳酸钙,现将此样品在高温下充分煅烧至反应完全反应,所得固体的质量是原样品的质量的 %.
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:碳酸钙受热分解生成氧化钙和二氧化碳,根据样品的质量可以计算碳酸钙的质量,根据碳酸钙的质量可以计算反应生成氧化钙和二氧化碳的质量,进一步可以计算所得固体的质量是原样品的质量质量分数.
解答:解:设样品的质量为m,反应生成二氧化碳的质量是x,
CaCO3
CaO+CO2↑,
100 44
m×25% x
=
,
x=0.11m,
所得固体的质量为:m-0.11m=0.89m,
所得固体质量是原样品质量的质量分数为:
×100%=89%,
故填:89.
CaCO3
| ||
100 44
m×25% x
| 100 |
| m×25% |
| 44 |
| x |
x=0.11m,
所得固体的质量为:m-0.11m=0.89m,
所得固体质量是原样品质量的质量分数为:
| 0.89m |
| m |
故填:89.
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案
相关题目
下列各组溶液中不用其他试剂,仅用组内的物质相互反应就能鉴别的是( )
| A、NaOH FeCl3 MgCl2 |
| B、Na2SO4 BaCl2 Na2CO3 |
| C、KNO3 CuSO4 NaCl |
| D、NaNO3 BaCl2 KCl |
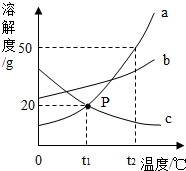 如图是三种固体物质a、b、c的溶解度曲线.
如图是三种固体物质a、b、c的溶解度曲线.