题目内容
一包不纯的Na2CO3固体,其杂质可能是CaCl2、NaCl、NaHCO3中的一种或几种.现取该样品,溶于水得到澄清溶液;另取样品10.6g,加入100g稀盐酸恰好完全反应,产生气体4g,则下列判断正确的是( )
| A.加水得澄清溶液,样品中一定没有CaCl2 |
| B.样品中一定含有NaHCO3,可能含有NaCl |
| C.样品中一定含有NaCl,可能含有NaHCO3 |
| D.所加的稀盐酸溶质质量分数不大于7.3% |
ACD
解析试题分析:由于碳酸钠和氯化钙能够生成白色的碳酸钙沉淀,而取该样品,溶于水得到澄清溶液,所以固体中一定不会含有氯化钙,假设该固体都是碳酸钠,则设生成的二氧化碳的质量是x反应的氯化氢的质量是y
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 73 44
10.6g y x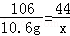 =
=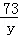
x=4.4g y=7.3g
由于杂质是碳酸氢钠也能生成二氧化碳,且碳酸氢钠的相对分子质量比碳酸钠小,所以同质量的碳酸氢钠比碳酸钠生成的二氧化碳要多,故杂质中不能全部是碳酸氢钠,故还一定含有氯化钠,且杂质可以全部是氯化钠,也可以是氯化钠和碳酸氢钠两者都有;
如果该固体全部是碳酸钠,此时盐酸的溶质质量分数是 ×100%=7.3%,而反应中的二氧化碳小于4.4g,所以消耗的氯化氢应该比此时要少,所以所加的稀盐酸溶质质量分数不大于7.3%;
×100%=7.3%,而反应中的二氧化碳小于4.4g,所以消耗的氯化氢应该比此时要少,所以所加的稀盐酸溶质质量分数不大于7.3%;
故选ACD
考点:物质的鉴别、推断;酸的化学性质;根据化学反应方程式的计算.
点评:熟练掌握碳酸盐的性质,学会利用利用极端假设法来解答这类题目:先假设全部是主要的物质,然后根据计算的数据,判断是否含有其他的物质,这是解答此题的关键.

将17.4g部分变质的氢氧化钙,加入到200g7.3%的稀盐酸中,恰好完全反应,则所得溶液中溶质的质量为
| A.11.1g | B.14.2g | C.22.2g | D.44.4g |
把12g某固体放入90g水中充分溶解后过滤,滤出该固体2g,则该滤液的溶质质量分数是
| A.10% | B.11.7% | C.12% | D.13.3% |
在某H2O2溶液中氢元素与氧元素的质量比为2:17,现向19g该H2O2溶液中加入1g二氧化锰,充分反应后,生成氧气的质量为
( )
| A.1g | B.1.6g | C.4.2g | D.8.5g |