题目内容
【题目】(1) 用化学符号表示:
①氢原子______________ ②干冰_________
③空气中含量最高的物质_____ ④构成氯化钠的阳离子______
(2) 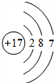 是某元素的原子结构示意图,该原子的质子数为 ______,原子的核外有________个电子层,在化学反应中容易_____________电子(填“得到” 或“失去”)。
是某元素的原子结构示意图,该原子的质子数为 ______,原子的核外有________个电子层,在化学反应中容易_____________电子(填“得到” 或“失去”)。
(3) 写出下列反应的符号表达式,并回答有关问题。
①铁丝在氧气中燃烧:_______________________
②有水生成的化合反应:_____________________________________。
③铜绿受热分解:____________________,固体的颜色变化:_____________
【答案】 H CO2 N2 Na+ 17 3 得到 Fe+O2![]() Fe3O4 H2+O2
Fe3O4 H2+O2![]() H2O Cu2(OH)2CO3
H2O Cu2(OH)2CO3![]() CuO+H2O+CO2↑ 绿色变为黑色
CuO+H2O+CO2↑ 绿色变为黑色
【解析】(1) ①氢原子可直接用元素符号表示;②干冰是二氧化碳,应用CO2表示。
③空气中含量最高的物质是氮气,符号为N2;④构成氯化钠的阳离子为钠离子,符号为Na+;
(2) 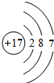 是某元素的原子结构示意图,该原子的质子数为17,原子的核外有3个电子层,其最外层有7个电子,在化学反应中容易得到电子。
是某元素的原子结构示意图,该原子的质子数为17,原子的核外有3个电子层,其最外层有7个电子,在化学反应中容易得到电子。
(3) 写出下列反应的符号表达式,并回答有关问题。
①铁丝在氧气中燃烧:铁丝在氧气中燃烧生成四氧化三铁:Fe+O2![]() Fe3O4。
Fe3O4。
②有水生成的化合反应:应该是氢气在氧气中燃烧生成水:H2+O2![]() H2 O。
H2 O。
③铜绿受热分解:铜绿为Cu2(OH)2CO3,Cu2(OH)2CO3![]() CuO+H2O+CO2↑,固体的颜色变化为由绿色变为黑色(氧化铜)。
CuO+H2O+CO2↑,固体的颜色变化为由绿色变为黑色(氧化铜)。

 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案【题目】某校化学兴趣小组在老师指导下,进行了“影响双氧水分解因素”的实验。以下是探究影响化学反应快慢因素的相关数据(常温通常指20℃;“浓度”指溶质的质量分数)
实验序号 | 过氧化氢溶液浓度/% | 过氧化氢溶液质量/g | 温度/℃ | 二氧化锰用量/g | 氧气体积/ml | 反应所需时间/s |
① | 5 | 12 | 20 | 0.2 | 125 | 11 |
② | 30 | 12 | 20 | 0.2 | 125 | 2 |
③ | 30 | 12 | 40 | / | 125 | 148 |
④ | 30 | 12 | 90 | / | 125 | 82 |
(1)通过实验①和②对比可知,化学反应快慢与_________有关;
(2)通过对比实验_______和________可知,化学反应快慢与温度的关系是:相同条件下,温度_______,反应速率越快。
(3)由上述实验可知,实验室用过氧化氢制取氧气的最合适的条件是:温度为________℃,过氧化氢的浓度为____% ,二氧化锰_______(填“有”或“无”)。
(4)实验中除了量筒外,还需要用到的测量仪器有:_______。
(5)为完成本实验,收集装置可以选下图中的 __________(填序号)