题目内容
【题目】以某矿山酸性废水(主要含硫酸、硫酸铁、硫酸铜和硫酸锌等)为原料,通过下述流程可将废水中的铁、铜和锌分步沉淀,实现回收利用。
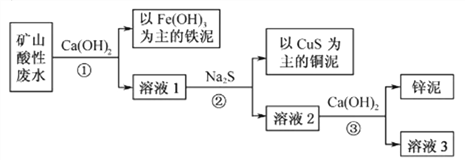
(1)步骤①中,加入Ca(OH)2有两个作用。
一是中和废水中的硫酸,该反应的化学方程式为___________________________;
二是将硫酸铁转化为Fe(OH)3,该反应属于______________________(填基本反应类型)。
(2)步骤③中,锌泥中最主要的含锌化合物的化学式为___________________;
(3)为分步回收铁、铜、锌等金属资源且直接得到铜单质,只需改变上述流程中的某步骤加入的试剂即可。该步骤和应加入的试剂分别是____________。
【答案】 Ca(OH)2+ H2SO4=CaSO4+ 2H2O 复分解反应 Zn(OH)2 步骤② 锌
【解析】(1)根据氢氧化钙与硫酸反应生成硫酸钙和水解答;根据两种化合物互相交换成分,生成另外两种化合物且生成物中有气体、沉淀或水生成解答;(2)根据硫酸锌与氢氧化钙反应生成氢氧化锌解答;(3)根据锌能置换出硫酸铜溶液中的铜解答。(1)氢氧化钙与硫酸反应生成硫酸钙和水,反应的化学方程式为Ca(OH)2+ H2SO4=CaSO4+ 2H2O;由反应的化学方程式3Ca(OH)2+ Fe2(SO4)3=3CaSO4+ 2Fe(OH)3↓可知,该反应属于复分解反应;(2)硫酸锌与氢氧化钙反应生成氢氧化锌,故锌泥中最主要的含锌化合物的化学式为Zn(OH)2;(3)锌能置换出硫酸铜溶液中的铜,故在步骤②中加入锌即可。

【题目】已知氯化钾、硝酸钾在不同温度时的溶解度如下表:
温度/℃ | 0 | 20 | 40 | 60 | |
溶解度/g | 氯化钾 | 27.6 | 34.0 | 40.0 | 45.5 |
硝酸钾 | 13.3 | 31.6 | 63.9 | 110.0 | |
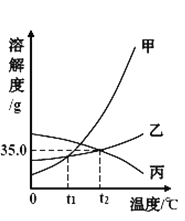
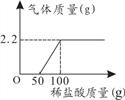
依据上表数据和溶解度曲线判断,下列说法错误的是
A. 能表示硝酸钾和氯化钾的溶解度曲线分别是甲和乙
B. t1℃时,氯化钾和硝酸钾的溶解度相等,在 34.0 g 至 35.0 g 之间
C. t2℃时,将接近饱和的丙物质的溶液升高温度,可使其变成饱和溶液
D. 氯化钾中混有少量的硝酸钾,可采用降温结晶的方法提纯