题目内容
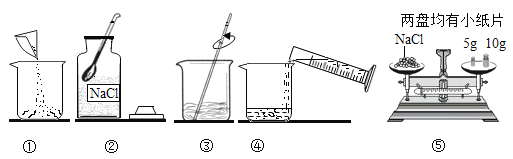
【题目】将盛有等质量、等质量分数且足量的稀盐酸的两只烧杯,放在托盘天平的左右两盘,天平平衡。在左盘烧杯中加入10克碳酸钙,若要使天平重新平衡,则右盘烧杯中应加入的物质可能是
A.10克碳酸钾和碳酸钠B.10克碳酸镁和碳酸钠
C.10克氧化铜D.10克镁粉和铜粉
【答案】B
【解析】
加入10g碳酸钙,设左盘增加的质量为x
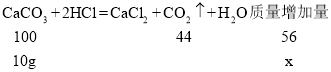
![]() x=5.6g
x=5.6g
A、碳酸钾和稀盐酸反应:![]() ,碳酸钾的相对分子质量是138,由化学方程式可知,如果10g全部是碳酸钾,生成二氧化碳的质量小于4.4g, 质量增加量大于5.6g;
,碳酸钾的相对分子质量是138,由化学方程式可知,如果10g全部是碳酸钾,生成二氧化碳的质量小于4.4g, 质量增加量大于5.6g;
碳酸钠和稀盐酸反应:![]() ,碳酸钠的相对分子质量是106,由化学方程式可知,如果10g全部是碳酸钠,生成二氧化碳的质量小于4.4g, 质量增加量大于5.6g;
,碳酸钠的相对分子质量是106,由化学方程式可知,如果10g全部是碳酸钠,生成二氧化碳的质量小于4.4g, 质量增加量大于5.6g;
故无论碳酸钾和碳酸钠以何种比例混合,天平都不会平衡,不符合题意;
B、碳酸镁和稀盐酸反应:![]() ,如果10g全部是碳酸镁,碳酸镁的相对分子质量是84,由化学方程式可知,如果10g全部是碳酸镁,生成二氧化碳的质量大于4.4g, 质量增加量小于5.6g;由A可知,如果10g全部是碳酸钠,质量增加量大于5.6g,故天平可能会平衡,符合题意;
,如果10g全部是碳酸镁,碳酸镁的相对分子质量是84,由化学方程式可知,如果10g全部是碳酸镁,生成二氧化碳的质量大于4.4g, 质量增加量小于5.6g;由A可知,如果10g全部是碳酸钠,质量增加量大于5.6g,故天平可能会平衡,符合题意;
C、氧化铜与稀盐酸反应生成氯化铜和水,无气体生成,右盘增加量就是10g,天平不平衡,不符合题意;
D、假设10g全部是镁粉,镁与稀盐酸反应:![]() , 生成氢气的质量小于4.4g,质量增加量一定大于5.6g,铜与稀盐酸不反应,故无论镁粉和铜粉以何种比例混合,质量增加量都大于5.6g,天平不会平衡,不符合题意。
, 生成氢气的质量小于4.4g,质量增加量一定大于5.6g,铜与稀盐酸不反应,故无论镁粉和铜粉以何种比例混合,质量增加量都大于5.6g,天平不会平衡,不符合题意。
故选B。

【题目】某化学兴趣小组欲测定某氯化镁样品中MgCl2的含量(杂质为NaCl),甲、乙、丙三位同学分别取10g样品溶于一定量的水中,得到45.8g、45.8g、50g三份样品溶液,再分别加入溶质质量分数相同的氢氧化钠溶液,所得实验数据如表:
甲同学 | 乙同学 | 丙同学 | |
所用样品溶液质量(g) | 45.8 | 45.8 | 50 |
加入氢氧化钠溶液质量(g) | 70 | 60 | 60 |
反应得到沉淀的质量(g) | 5.8 | 5.8 | 5.8 |
试回答下列问题:
(1) 同学的实验数据显示了MgCl2和NaOH恰好完全反应。
(2)计算MgCl2和NaOH恰好完全反应时所得溶液溶质的质量分数。(结果精确到0. 1%)
【题目】下列图象能正确反映对应变化关系的是( )
|
|
|
|
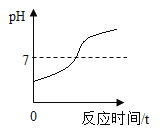
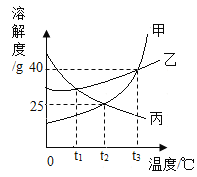
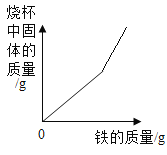
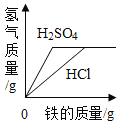
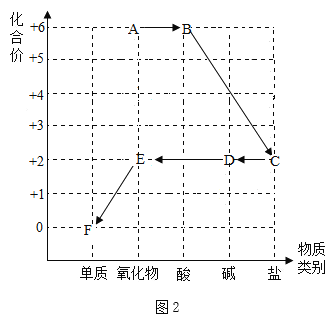
A.向100g 10%的稀盐酸中逐滴加入100g 10%的氢氧化钠溶液 | B.将t3℃时等质量的甲、乙、丙的饱和溶液分别降温到t1℃,所得溶液的质量丙>乙>甲 | C.向盛有一定量硫酸铜溶液的烧杯中逐渐加入铁粉至过量 | D.向等质量等浓度的稀硫酸和稀盐酸中各加入铁粉至过量 |
A.AB.BC.CD.D
【题目】将氯化钠和氯化铁的固体混合物40g完全溶于101.4g水中形成溶液,再将100g一定溶质质量分数的氢氧化钠溶液分5次加入到该溶液中,充分反应后,测得的实验数据如下表所示:
实验次数 | 1 | 2 | 3 | 4 | 5 |
加入氢氧化钠溶液质量/g | 20 | 20 | 20 | 20 | 20 |
共生成沉淀的质量/g | 5.35 | 10.7 | m | 21.4 | 21.4 |
求:(1)表中m的值为________。
(2)原混合物中氯化铁的质量___________。
(3)恰好完全反应时,所得溶液的溶质质量分数是____。(写出计算过程,结果精确到0.1%)