题目内容
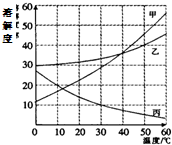 (2011?崇明县二模)甲、乙、丙三种固体物质(不含结晶水)的溶解度曲线如图所示.
(2011?崇明县二模)甲、乙、丙三种固体物质(不含结晶水)的溶解度曲线如图所示.据图回答:
(1)50℃时,乙物质的溶解度是
40
40
g/100g水;(2)20℃时,三种物质的溶解度由大到小的顺序为
乙>甲>丙
乙>甲>丙
;(3)将50℃时甲、乙、丙三种物质的饱和溶液温度降低到10℃,此时溶液中溶质质量分数最小的物质是
丙
丙
;(4)实验室需要配制15%的甲溶液.现有30g甲固体,能配制甲溶液
200
200
g.配制甲溶液时,有下列操作:①溶解;②称取氯化钠固体;③计算;④量取蒸馏水.正确的操作顺序是B
B
.(填序号)A.①②③④B.③②④①C.③①②④D.③②①④
分析:(1)根据溶解度的查法考虑;
(2)根据某一温度时物质溶解度的比较方法考虑;
(3)根据50℃时甲、乙、丙三种物质的饱和溶液温度降低到10℃溶质质量分数的变化考虑;
(4)根据溶质质量分数、溶质质量、溶液质量三者的关系,溶液配制的步骤考虑本题.
(2)根据某一温度时物质溶解度的比较方法考虑;
(3)根据50℃时甲、乙、丙三种物质的饱和溶液温度降低到10℃溶质质量分数的变化考虑;
(4)根据溶质质量分数、溶质质量、溶液质量三者的关系,溶液配制的步骤考虑本题.
解答:解:(1)从50℃向上作垂线,与乙物质的曲线的交点再向纵坐标作垂线,所指的数值就是该温度下的溶解度;
(2)从20℃向上做垂线,与曲线的交点在上面的溶解度就大,所以20℃时它们的溶解度大小顺序是乙>甲>丙;
(3)由于饱和溶液的质量分数与溶解度有关,溶解度大的溶质质量分数就大,所以在50℃时甲、乙、丙三种物质的饱和溶液的质量分数大小是:甲>乙>丙,温度降低到10℃,甲和乙都析出晶体仍然饱和,但10℃乙的溶解度大于甲的,所以此时乙的溶质质量分数大于甲的,丙降温后变为不饱和,所以溶质质量分数不变,主要比较一下甲在10℃时溶解度与丙在50℃的溶解度大小就行,通过比较丙是小的,所以溶质质量分数最小的是丙;
(4)甲溶液质量:
=200g;配制溶液的基本步骤:计算、称量、量取、溶解、装瓶存放.
故答案为:(1)40;(2)乙>甲>丙;(3)丙;(4)200g;B.
(2)从20℃向上做垂线,与曲线的交点在上面的溶解度就大,所以20℃时它们的溶解度大小顺序是乙>甲>丙;
(3)由于饱和溶液的质量分数与溶解度有关,溶解度大的溶质质量分数就大,所以在50℃时甲、乙、丙三种物质的饱和溶液的质量分数大小是:甲>乙>丙,温度降低到10℃,甲和乙都析出晶体仍然饱和,但10℃乙的溶解度大于甲的,所以此时乙的溶质质量分数大于甲的,丙降温后变为不饱和,所以溶质质量分数不变,主要比较一下甲在10℃时溶解度与丙在50℃的溶解度大小就行,通过比较丙是小的,所以溶质质量分数最小的是丙;
(4)甲溶液质量:
| 30g |
| 15% |
故答案为:(1)40;(2)乙>甲>丙;(3)丙;(4)200g;B.
点评:通过回答本题知道了溶解度曲线表示的意义,知道了溶解度如何比较大小,饱和溶液溶质质量分数的计算方法.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目