题目内容
(2011?崇明县二模)如图是化学实验中常用的几种装置.
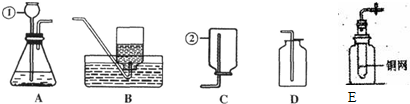
请回答下列问题:
(1)指出有编号的仪器名称:①
(2)利用上述A、D装置的组合制取O2时的化学反应方程式为
(3)E装置是用底部有破洞的试管和广口瓶组装成的制取CO2的发生装置,该装置的优点是
(4)装置A也可以用来制取CO2.如果选用碳酸钠粉末和稀盐酸来制取CO2,为了控制反应速率,应对装置A作如何改进?(可另增仪器)请你至少写出一种方案
(5)为比较二氧化碳和空气的温室效应,可将盛满两种气体的密闭广口瓶同时置于阳光下进行实验.此实验需定时测量的数据是
(6)实验室常用氯酸钾和二氧化锰混合制氧气,现把3.45g混合固体装入试管中加热,完全反应后停止加热,待试管冷却后,称得试管内的固体剩余物为2.49g.
计算:
①反应结束后,理论上得到氧气的物质的量是
②3.45g混合固体中氯酸钾有多少克?(写出计算过程)

请回答下列问题:
(1)指出有编号的仪器名称:①
长颈漏斗
长颈漏斗
,②集气瓶
集气瓶
;(2)利用上述A、D装置的组合制取O2时的化学反应方程式为
2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
,用带火星的木条放在D装置瓶口检验O2是否收集满,是利用了氧气
| ||
密度比空气大和助燃
密度比空气大和助燃
的性质;(3)E装置是用底部有破洞的试管和广口瓶组装成的制取CO2的发生装置,该装置的优点是
随时控制反应的进行或停止
随时控制反应的进行或停止
;若将制得的CO2通入澄清石灰水中,始终未出现浑浊现象,可能的原因是生成的二氧化碳中混有氯化氢气体(或盐酸浓度较高,挥发出了氯化氢气体或石灰水变质或二氧化碳的量很少)
生成的二氧化碳中混有氯化氢气体(或盐酸浓度较高,挥发出了氯化氢气体或石灰水变质或二氧化碳的量很少)
;(4)装置A也可以用来制取CO2.如果选用碳酸钠粉末和稀盐酸来制取CO2,为了控制反应速率,应对装置A作如何改进?(可另增仪器)请你至少写出一种方案
将长颈漏斗改用分液漏斗(或将长颈漏斗改用注射器或将长颈漏斗改用胶头滴管或将长颈漏斗下端插入小试管中)
将长颈漏斗改用分液漏斗(或将长颈漏斗改用注射器或将长颈漏斗改用胶头滴管或将长颈漏斗下端插入小试管中)
;(5)为比较二氧化碳和空气的温室效应,可将盛满两种气体的密闭广口瓶同时置于阳光下进行实验.此实验需定时测量的数据是
温度
温度
;(6)实验室常用氯酸钾和二氧化锰混合制氧气,现把3.45g混合固体装入试管中加热,完全反应后停止加热,待试管冷却后,称得试管内的固体剩余物为2.49g.
计算:
①反应结束后,理论上得到氧气的物质的量是
0.03
0.03
mol;②3.45g混合固体中氯酸钾有多少克?(写出计算过程)
分析:(1)根据实验室常见仪器的名称进行解答;
(2)根据实验室制取氧气的反应原理,反应装置为固液不加热,反应物为过氧化氢和二氧化锰;D装置瓶口检验O2是利用氧气密度比空气大和助燃的性质;
(3)根据气压的原理进行解答;CO2通入澄清石灰水中,始终未出现浑浊现象,分析实验现象解答;
(4)用碳酸钠粉末和稀盐酸来制取CO2,为了控制反应速率,必须控制液体的加入,可改用分液漏斗等装置;
(5)比较二氧化碳和空气的温室效应,即比较温度;
(6)根据质量守恒定律可求理论上得到氧气的物质的量;根据化学方程式计算3.45g混合固体中氯酸钾的质量.
(2)根据实验室制取氧气的反应原理,反应装置为固液不加热,反应物为过氧化氢和二氧化锰;D装置瓶口检验O2是利用氧气密度比空气大和助燃的性质;
(3)根据气压的原理进行解答;CO2通入澄清石灰水中,始终未出现浑浊现象,分析实验现象解答;
(4)用碳酸钠粉末和稀盐酸来制取CO2,为了控制反应速率,必须控制液体的加入,可改用分液漏斗等装置;
(5)比较二氧化碳和空气的温室效应,即比较温度;
(6)根据质量守恒定律可求理论上得到氧气的物质的量;根据化学方程式计算3.45g混合固体中氯酸钾的质量.
解答:解:(1)根据实验室常见仪器的名称可知:①长颈漏斗;②集气瓶;
(2)根据实验室制取氧气的反应原理,反应装置为固液不加热,反应物为过氧化氢和二氧化锰,化学方程式
为:2H2O2
2H2O+O2↑;D装置瓶口检验O2是利用氧气密度比空气大和助燃的性质;
(3)根据气压的原理,E装置装置的优点是:随时控制反应的进行或停止;
CO2通入澄清石灰水中,始终未出现浑浊现象,可能的原因是:生成的二氧化碳中混有氯化氢气体(或盐酸浓度较高,挥发出了氯化氢气体或石灰水变质或二氧化碳的量很少);
(4)用碳酸钠粉末和稀盐酸来制取CO2,为了控制反应速率,必须控制液体的加入,因此对装置A作改进方法为:将长颈漏斗改用分液漏斗或将长颈漏斗改用注射器或将长颈漏斗改用胶头滴管或将长颈漏斗下端插入小试管中;
(5)比较二氧化碳和空气的温室效应,即比较温度;
(6)①根据质量守恒定律可求理论上得到氧气的质量为:3.45g-2.49g=0.96g;
得到氧气的物质的量为:
=0.03 mol;
②解:设混合物有xmol氯酸钾分解产生0.03mol氧气
2KClO3
2KCl+3O2↑
2 3
x 0.03mol
=
x=0.02 mol
氯酸钾的质量为:0.02mol×122.5g/mol=2.45g
答:混合物中氯酸钾的质量为2.45g.
故答案为:(1)长颈漏斗; 集气瓶;
(2)2H2O2
2H2O+O2↑
密度比空气大和助燃(须同时指明“密度比空气大、助燃”关键词.缺一条件不得分);
(3)随时控制反应的进行或停止 生成的二氧化碳中混有氯化氢气体或(盐酸浓度较高,挥发出了氯化氢气体或石灰水变质或二氧化碳的量很少)其他合理均可;
(4)将长颈漏斗改用分液漏斗或将长颈漏斗改用注射器或将长颈漏斗改用胶头滴管或将长颈漏斗下端插入小试管中其他合理均可;
(5)温度;
(6)0.03mol;
解:设混合物有xmol氯酸钾分解产生0.03mol氧气
2KClO3
2KCl+3O2↑
2 3
x 0.03mol
=
x=0.02 mol
氯酸钾的质量为:0.02mol×122.5g/mol=2.45g
答:混合物中氯酸钾的质量为2.45g
(2)根据实验室制取氧气的反应原理,反应装置为固液不加热,反应物为过氧化氢和二氧化锰,化学方程式
为:2H2O2
| ||
(3)根据气压的原理,E装置装置的优点是:随时控制反应的进行或停止;
CO2通入澄清石灰水中,始终未出现浑浊现象,可能的原因是:生成的二氧化碳中混有氯化氢气体(或盐酸浓度较高,挥发出了氯化氢气体或石灰水变质或二氧化碳的量很少);
(4)用碳酸钠粉末和稀盐酸来制取CO2,为了控制反应速率,必须控制液体的加入,因此对装置A作改进方法为:将长颈漏斗改用分液漏斗或将长颈漏斗改用注射器或将长颈漏斗改用胶头滴管或将长颈漏斗下端插入小试管中;
(5)比较二氧化碳和空气的温室效应,即比较温度;
(6)①根据质量守恒定律可求理论上得到氧气的质量为:3.45g-2.49g=0.96g;
得到氧气的物质的量为:
| 0.96g |
| 32g/mol |
②解:设混合物有xmol氯酸钾分解产生0.03mol氧气
2KClO3
| ||
| △ |
2 3
x 0.03mol
| 2 |
| x |
| 3 |
| 0.03mol |
氯酸钾的质量为:0.02mol×122.5g/mol=2.45g
答:混合物中氯酸钾的质量为2.45g.
故答案为:(1)长颈漏斗; 集气瓶;
(2)2H2O2
| ||
密度比空气大和助燃(须同时指明“密度比空气大、助燃”关键词.缺一条件不得分);
(3)随时控制反应的进行或停止 生成的二氧化碳中混有氯化氢气体或(盐酸浓度较高,挥发出了氯化氢气体或石灰水变质或二氧化碳的量很少)其他合理均可;
(4)将长颈漏斗改用分液漏斗或将长颈漏斗改用注射器或将长颈漏斗改用胶头滴管或将长颈漏斗下端插入小试管中其他合理均可;
(5)温度;
(6)0.03mol;
解:设混合物有xmol氯酸钾分解产生0.03mol氧气
2KClO3
| ||
| △ |
2 3
x 0.03mol
| 2 |
| x |
| 3 |
| 0.03mol |
氯酸钾的质量为:0.02mol×122.5g/mol=2.45g
答:混合物中氯酸钾的质量为2.45g
点评:本题主要考查学生运用所学化学知识综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目