题目内容
【题目】取0.18g炭在一定量氧气中燃烧,全部转化为一氧化碳和二氧化碳的混合气体.将混合气体通入足量石灰水中,充分反应后,得到0.5g碳酸钙.计算:
(1)混合气体中二氧化碳的质量_____.
(2)混合气体中一氧化碳的质量分数_____.
【答案】0.22g 56%
【解析】
考查利用化学方程式的计算。
(1)设二氧化碳的质量为x,则:
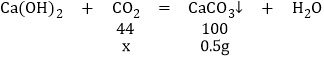
![]()
解得:x=0.22g;
(2)二氧化碳中碳元素的质量为:0.22g×![]() ×100%=0.06g
×100%=0.06g
所以一氧化碳的质量为:(0.18g﹣0.06g)÷![]() ×100%=0.28g
×100%=0.28g
所以一氧化碳的质量分数为:![]() ×100%=56%
×100%=56%
答:(1)混合气体中二氧化碳的质量为0.22g;
(2)混合气体中一氧化碳的质量分数为56%。

练习册系列答案
相关题目
【题目】甲、乙、丙、丁四种物质的相互反应关系如图所示,“—”表示相连的物质间能发生反应,下列符合对应反应关系的选项是

选项 | A | B | C | D | |
物 质 | 甲 | Ca(OH)2 | CO2 | H2 | Mg |
乙 | Na2CO3 | NaOH | O2 | HCl | |
丙 | H2SO4 | CaCl2 | CuO | CuSO4 | |
丁 | BaCl2 | K2CO3 | HCl | NaOH | |
A. AB. BC. CD. D