题目内容
【题目】鸡蛋壳的主要成分是碳酸钙。为了测定鸡蛋壳中钙元素的质量分数,某化学兴趣小组的甲同学提出:将鸡蛋壳洗净、干燥并研碎后,称取10g放在烧杯里,然后往烧杯中滴加足量的稀盐酸;乙同学提出要达到实验目的,还需在甲同学的实验过程中测定反应产生的气体质量。按要求回答下列问题![]() 假设鸡蛋壳中其它物质不与盐酸反应
假设鸡蛋壳中其它物质不与盐酸反应![]() 。
。
![]() 鸡蛋壳加入稀盐酸时发生的化学反应方程式______;
鸡蛋壳加入稀盐酸时发生的化学反应方程式______;
![]() 简述测定反应产生气体质量的方法______;
简述测定反应产生气体质量的方法______;
![]() 若实验过程中测得产生气体的质量为mg,则上述鸡蛋壳样品中钙元素的质量分数为______
若实验过程中测得产生气体的质量为mg,则上述鸡蛋壳样品中钙元素的质量分数为______![]() 用含m的代数式表示
用含m的代数式表示![]() ;
;
![]() 丙同学提出的下列因素会导致实验测定的结果偏高的是______。
丙同学提出的下列因素会导致实验测定的结果偏高的是______。
A.盐酸浓度偏大![]() 鸡蛋壳未研碎
鸡蛋壳未研碎![]() 鸡蛋壳未晾干
鸡蛋壳未晾干
【答案】![]() 称量反应前后装置的总质量
称量反应前后装置的总质量 ![]() A
A
【解析】
![]() 鸡蛋壳的主要成分是碳酸钙,碳酸钙与盐酸反应生成氯化钙、水和二氧化碳;故填:
鸡蛋壳的主要成分是碳酸钙,碳酸钙与盐酸反应生成氯化钙、水和二氧化碳;故填:![]() ;
;
![]() 反应生成的二氧化碳气体会逸散到空气中,造成装置的总质量减少,所以可以通过称量反应前后装置的总质量来测定反应生成气体的质量;故填:称量反应前后装置的总质量;
反应生成的二氧化碳气体会逸散到空气中,造成装置的总质量减少,所以可以通过称量反应前后装置的总质量来测定反应生成气体的质量;故填:称量反应前后装置的总质量;
![]() 设钙元素的质量为x,由化学方程式
设钙元素的质量为x,由化学方程式![]() 可得如下关系:
可得如下关系:
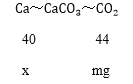
![]()
![]()
上述鸡蛋壳样品中钙元素的质量分数为![]() ;故填:
;故填:![]() ;
;
![]() 盐酸浓度偏大会挥发出氯化氢气体,造成减少的质量偏大,计算出的钙元素质量偏大,测定结果偏大,故A正确;
盐酸浓度偏大会挥发出氯化氢气体,造成减少的质量偏大,计算出的钙元素质量偏大,测定结果偏大,故A正确;
B、鸡蛋壳未研碎反应时间较长,对测定结果无明显影响,故B错误;
C、鸡蛋壳未晾干会造成测定结果偏小,故C错误。故填:A。

 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案【题目】如表为元素周期表的一部分,请利用数字①﹣⑤所表示元素完成下列问题。
① | He | ||||||
② | ③ | Ne | |||||
④ | ⑤ | Ar | |||||
(1)写出一种酸的化学式_____;
(2)由①、③两种元素组成,且元素③呈﹣1价的物质的化学式为_____;
(3)用化学用语表示:一种不溶性碱中金属元素的化合价_____;
(4)由①、③、④三种元素组成的物质能使紫色石蕊试液变为_____(填颜色)。