题目内容
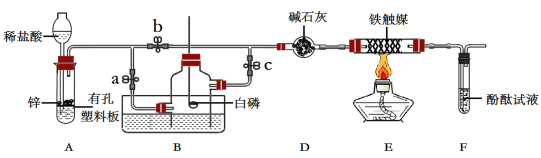
【题目】氨对工业及国防具有重要意义,化学小组的同学设计了如下图所示的装置用于制取少量氨气。
完成以下实验操作中的相关问题:
(1)检查装置气密性。
(2)关闭a、c,打开b,从长颈漏斗加入稀盐酸,A中发生反应的化学方程式为 。在F的出口处收集氢气并验纯。
(3)关闭c,在盛满空气的多孔玻璃钟罩内用激光点燃足量的白磷。反应的化学方程式为 。其目的是 。
(4)待多孔玻璃钟罩冷却到室温,打开a,观察到的现象是 。
(5)点燃酒精灯加热玻璃管E,并打开C。氢气和氮气在铁触媒的催化作用下生成氨气,反应的化学方程式为 。实验过程中D装置的作用是 。
【答案】(2)Zn+2HCl=ZnCl2+H2↑(3)4P + 5O2 点燃 2P2O5 除去空气中的氧气,以获得较纯净的氮气
(4)A中稀盐酸流入试管中与锌反应产生气泡,B中钟罩内液面下降
(5)N2 + 3H2 ![]() 2NH3 吸收二氧化碳、水蒸气和氯化氢
2NH3 吸收二氧化碳、水蒸气和氯化氢
【解析】
试题分析:(2)关闭a、c,打开b,从长颈漏斗加入稀盐酸,A中发生反应的化学方程式为Zn+2HCl=ZnCl2+H2↑(3)关闭c,在盛满空气的多孔玻璃钟罩内用激光点燃足量的白磷。反应的化学方程式为4P + 5O2 点燃 2P2O5其目的是除去空气中的氧气,以获得较纯净的氮气;(4)待多孔玻璃钟罩冷却到室温,打开a,观察到的现象是A中稀盐酸流入试管中与锌反应产生气泡,B中钟罩内液面下降;(5)点燃酒精灯加热玻璃管E,并打开C。氢气和氮气在铁触媒的催化作用下生成氨气,反应的化学方程式为N2 + 3H2 ![]() 2NH3实验过程中D装置的作用是吸收二氧化碳、水蒸气和氯化氢
2NH3实验过程中D装置的作用是吸收二氧化碳、水蒸气和氯化氢

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目