题目内容
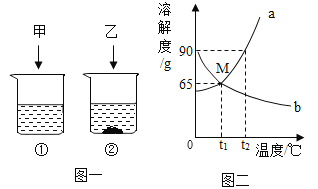
【题目】某化学兴趣小组的同学为了探究“复分解反应发生的条件”,做了如图两个实验:
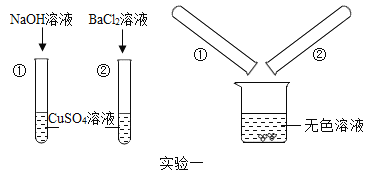
实验二
组合序号 | ③ | ④ | ⑤ |
组合的溶液 | H2SO4 NaOH | H2SO4 NaCl | H2SO4 Na2CO3 |
(实验一):
把试管①②中静置后的上层清液倒入洁净的烧杯中,最后只得到蓝色沉淀和无色溶液。
(1)写出混合后得到蓝色沉淀一定发生反应的化学方程式 _________。
(2)混合后所得无色溶液中一定含有的溶质是_______(填化学式,下同)可能含有的溶质是_________。请你设计实验证明混合后所得的无色溶液中可能含有的物质存在:
实验操作 | 实验现象 | 实验结论 |
取反应后的溶液少量于试管 中,向其中加入________ | ________ | 可能含有的物质存在 |
(实验二):
(3)在组合③、④、⑤中,组合_____无明显现象,但它们的实质不同,为了证明实质不同,小夕在实验过程中使用了酚酞试液。
(4)实验结束后把3个组合反应后的溶液混合,混合后溶液也显无色。混合后所得溶液中除酚酞外,溶质的组成可能是_______(填化学式)。
(结论):
(5)复分解反应发生的条件是:生成物中有__________。
【答案】![]() NaCl、Na2SO4 NaOH 酚酞溶液/CuSO4溶液 变红/蓝色沉淀 ③④ NaCl、Na2SO4、H2SO4或NaCl、Na2SO4 沉淀或气体或者水
NaCl、Na2SO4 NaOH 酚酞溶液/CuSO4溶液 变红/蓝色沉淀 ③④ NaCl、Na2SO4、H2SO4或NaCl、Na2SO4 沉淀或气体或者水
【解析】
(1)把试管①②中静置后的上层清液倒入洁净的烧杯中,最后只得到蓝色沉淀和无色溶液,说明第①个试管中反应后氢氧化钠一定有剩余,即第①个试管反应后溶质是硫酸钠和氢氧化钠;第②个试管中氯化钡不能剩余,否则会产生白色沉淀,硫酸铜可能剩余,也可能不剩余,所以第②个试管中一定含有氯化铜,所以混合后得到蓝色沉淀一定发生反应的化学方程式是氢氧化钠和氯化铜反应生成氢氧化铜沉淀和氯化钠,即:CuCl2+2NaOH=Cu(OH)2↓+2NaCl;
故填:CuCl2+2NaOH=Cu(OH)2↓+2NaCl;
(2)氢氧化钠与硫酸铜反应生成氢氧化铜沉淀和硫酸钠,氢氧化钠与氯化铜反应生成氢氧化铜沉淀和氯化钠,氢氧化钠可能剩余,所以混合后所得无色溶液中一定含有的溶质是NaCl和Na2SO4;可能含有的溶质是NaOH;
取反应后的溶液少量于试管 中,向其中加入酚酞溶液,如果溶液变红,证明含有氢氧化钠;或取反应后的溶液少量于试管中,向其中加入CuSO4溶液,如果生成蓝色沉淀,证明含有氢氧化钠;
故填:NaCl、Na2SO4;NaOH;酚酞溶液/CuSO4溶液;变红/蓝色沉淀;
(3)③硫酸和氢氧化钠反应生成硫酸钠和水,反应现象不明显,④硫酸和氯化钠不发生反应,无明显现象;⑤硫酸和碳酸钠反应生成硫酸钠、水和二氧化碳,有气泡放出;
故填:③④;
(4)溶液无色,说明一定不显碱性,一定不含有氢氧化钠和碳酸钠,由于硫酸与氢氧化钠反应生成硫酸钠和水,碳酸钠与硫酸反应生成硫酸钠、水和二氧化碳,所以反应后溶液中一定含有硫酸钠,在第④个组合中含有氯化钠,氯化钠和其它物质不反应,所以溶质中还一定含有氯化钠,硫酸可能过量,可能恰好完全反应,所以除酚酞外溶质的组成可能是:Na2SO4和NaCl或Na2SO4、NaCl、H2SO4;
故填:Na2SO4和NaCl或Na2SO4、NaCl、H2SO4;
(5)复分解反应发生的条件是:生成物中有沉淀生成或气体放出或有水生成。
故填:沉淀或气体或者水。

 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案【题目】请从A~D中任选三个作答。
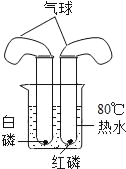
如图所示,在两支试管中进行实验,补全实验方案。
序号 | 目的 | 步骤 |
A | 验证_____ | ①试管1中加入一小块白磷和5mL80℃热水,试管2中加入一小块白磷和5mL冷水;②分别通入氧气 |
B | 鉴别稀硫酸和碳酸钠溶液 | ①试管1、2中分别加入两种待测溶液;②分别加入_____溶液 |
C | 比较铁、铜、银的金属活动性 | ①试管1中加入FeSO4溶液,试管2中加入AgNO3溶液; ②分别插入_____ |
D | 比较_____ | ①试管1中加入一粒高锰酸钾和5mL汽油,试管2中加入一粒碘和5mL汽油;②振荡 |
【题目】银白色的金属钠是化学实验室中常见的药品,其化学性质十分活泼。某化学兴趣小组的同学,进行如下探究活动。
[查阅资料]
将一小块银白色的金属钠放置在空气中会发生下列变化:
钠![]() 钠的氧化物
钠的氧化物![]() 氢氧化钠溶液
氢氧化钠溶液![]() 白色固体
白色固体
[查阅资料]
A.钠的氧化物有氧化钠(Na2O)和过氧化钠(Na2O2),都能与水反应,反应化学方程式
如:Na2O+H2O=2NaOH;2Na2O2+2H2O=4NaOH+O2↑
B.CaCl2溶液呈中性;碳酸钠溶液能与CaCl2溶液发生复分解反应;
C.碳酸钠溶液与盐酸反应方程式有:
Na2CO3 +HCl=NaHCO3 +NaCl(盐酸量不足)
Na2CO3+2HCl=2NaCl+H2O+CO2↑(盐酸量过量)
探究一:钠的氧化物是Na2O还是Na2O2 ?
(1)为检验常温下钠与氧气反应的产物,是Na2O还是Na2O2,完成实验方案:
选取试剂 | 实验现象 | 实验结论 |
__________ | __________ | 产物为Na2O |
探究二:白色固体是NaOH还是Na2CO3 ?
(2) 钠在空气中放置一段时间得到白色固体的成分
猜想1:Na2CO3 猜想2:NaOH 猜想3:Na2CO3和NaOH
[实验1] 取少量白色固体加水配成溶液,再滴入几滴稀盐酸,无气泡产生。
化学小组认为:据此现象,还不能得出猜想2成立。理由是________________。
[实验2] 化学小组进行如下实验
实验操作 | 实验现象 | 实验结论 |
①取少量白色固体配成溶液,加入足量______ | __________ | 猜想3成立 |
②过滤,取少量滤液滴入___________ | __________ |
【题目】科学贵在创新,以下是对部分化学实验的改进,其中不能达到目的是( )
A | B | |
改 进 后 实 验 |
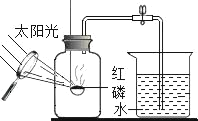
燃烧条件 |
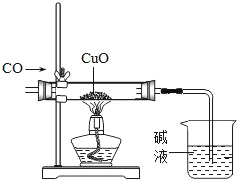
CO还原氧化剂 |
目的 | 防止燃烧产物污染空气 | 防止尾气对大气的污染 |
C | D | |
改 进 后 实 验 |
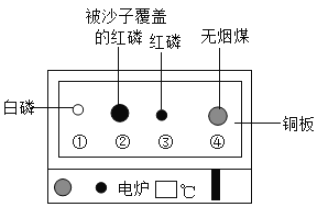
测定氧气含量 |
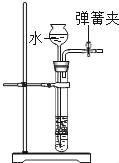
检验气密性 |
目的 | 不用酒精灯点燃,使测定结果更精确 | 现象更明显 |
A. AB. BC. CD. D