题目内容
实验室常用的干燥剂“碱石灰”是CaO和固体NaOH的混合物,极易与空气中水蒸气和CO2反应而变质。某同学对一瓶久置的“碱石灰”作了如下探究:
(1)【猜想】
猜想Ⅰ:没有变质,“碱石灰”只含有CaO、固体NaOH;
猜想Ⅱ:已完全变质,“碱石灰”全部变成了CaCO3和Na2CO3。
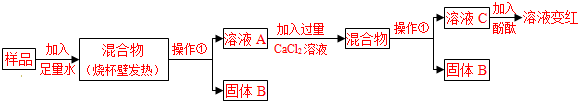
(2)【实验】如下图所示:
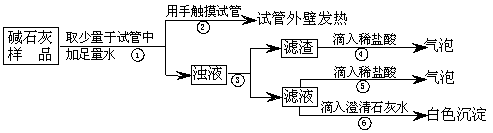 |
(3)【判断】
A.若Ca(OH)2、CaCO3和Na2CO3投入到水中不会放热,
则由操作②现象判断:猜想Ⅱ____ ___(填成立、不成立)
B.操作⑥发生化学反应的方程式为_____________ _________;
由操作⑤、⑥的现象判断:滤液中含有_________ __(写化学式);
由此判断猜想Ⅰ____ ___(填:成立、不成立)。
C.综合A和B的结论 ,判断该样品为 变质,(填部分或全部)
,判断该样品为 变质,(填部分或全部)
任写一个变质的化学方程式________________________________。
【拓展】由上述实验说明:实验室中“碱石灰”应_____保存;
操作③中玻璃棒的作用是 。
A.不成立
B.Ca(OH)2+Na2CO3==CaCO3↓+2NaOH
Na2CO3、不成立
C.部分变质,2NaOH + CO2 ==== Na2CO3 + H2O(合理即可)
密封保存;引流

练习册系列答案
相关题目




 碱石灰是实验室常用的干燥剂.同学们为确认一瓶久置的“碱石灰”(可能已部分变质或全部变质)样品的成分,进行如下探究.
碱石灰是实验室常用的干燥剂.同学们为确认一瓶久置的“碱石灰”(可能已部分变质或全部变质)样品的成分,进行如下探究.