题目内容
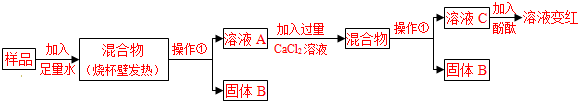
33、实验室常用的干燥剂“碱石灰”是CaO和NaOH固体的混合物.同学们为确认一瓶久置的“碱石灰”样品的成分,进行如图实验探究.

查阅资料:
a.Ca(OH)2、Na2CO3溶于水无明显的温度变化.
b.CaCl2+Na2CO3=2NaCl+CaCO3↓.
c.CaCl2溶液呈中性.
(1)滤渣B中一定含有
(2)滤液C成分的探究.
猜想:滤液C中的溶质可能为①NaOH;②Na2CO3;③NaOH和Na2CO3;④
设计方案并进行实验:甲、乙、丙同学分别设计如下方案并进行探究:
甲同学:取滤液C少许放入试管中,滴加足量的稀盐酸,产生大量无色气体,则滤液C中的溶质是Na2CO3.
乙同学:取滤液C少许放入试管中,滴加足量的无色酚酞,液体变成红色,则滤液C中的溶质一定含有NaOH.
丙同学:取滤液C少许放入试管中,滴加Ca(OH)2溶液,有白色沉淀产生.向上层清液中滴加无色酚酞,无色酚酞变成红色,则滤液C中的溶质是NaOH和Na2CO3.
反思与评价:
丁同学认真分析上述三位同学的实验,认为他们的结论均有不足之处,并且做出了正确的判断.
他认为滤液C中的溶质一定含有
为进一步确认猜想③正确,请你帮助他设计实验进行验证.
(3)实验过程中,同学们还发现向样品中加入足量水溶解时放出大量的热.综合对滤液和滤渣成分的探究,下列对样品成分的分析正确的是
①样品中一定含NaOH ②样品中一定含Na2CO3
③样品中含NaOH、CaO中的一种或两种.

查阅资料:
a.Ca(OH)2、Na2CO3溶于水无明显的温度变化.
b.CaCl2+Na2CO3=2NaCl+CaCO3↓.
c.CaCl2溶液呈中性.
(1)滤渣B中一定含有
CaCO3
,产生该物质的化学方程式可能是Ca(OH)2+Na2CO3=CaCO3↓+2NaOH或Ca(OH)2+CO2=CaCO3↓+H2O
(写出一个即可).(2)滤液C成分的探究.
猜想:滤液C中的溶质可能为①NaOH;②Na2CO3;③NaOH和Na2CO3;④
NaOH和Ca(OH)2
.设计方案并进行实验:甲、乙、丙同学分别设计如下方案并进行探究:
甲同学:取滤液C少许放入试管中,滴加足量的稀盐酸,产生大量无色气体,则滤液C中的溶质是Na2CO3.
乙同学:取滤液C少许放入试管中,滴加足量的无色酚酞,液体变成红色,则滤液C中的溶质一定含有NaOH.
丙同学:取滤液C少许放入试管中,滴加Ca(OH)2溶液,有白色沉淀产生.向上层清液中滴加无色酚酞,无色酚酞变成红色,则滤液C中的溶质是NaOH和Na2CO3.
反思与评价:
丁同学认真分析上述三位同学的实验,认为他们的结论均有不足之处,并且做出了正确的判断.
他认为滤液C中的溶质一定含有
Na2CO3
,可能含有NaOH.为进一步确认猜想③正确,请你帮助他设计实验进行验证.
| 实验操作 | 实验现象 | 实验结论及解释 |
| ① 取少量滤液C于试管中,加入足量CaCl2溶液 |
有白色沉淀生成 |
猜想③正确 |
| ② 过滤,在滤液中滴加无色酚酞试液 |
溶液由无色变成红色 |
②③
(填序号).①样品中一定含NaOH ②样品中一定含Na2CO3
③样品中含NaOH、CaO中的一种或两种.
分析:碱石灰变质的过程:(1)CaO和水反应生成氢氧化钙,然后氢氧化钙再空气中二氧化碳反应生成碳酸钙;(2)氢氧化钠吸水后潮解,然后会与空气中的二氧化碳反应生成碳酸钠.
解答:解:(1)由题给条件可知碱石灰变质后的可能会含有碳酸钙碳酸钠等物质.从实验方案中我们向滤渣中加入稀盐酸产生了气体,从而我们判断该滤渣中含有碳酸钙.碳酸钙产生的原因有两个可能:一个是CaO和水反应生成氢氧化钙,然后氢氧化钙再空气中二氧化碳反应生成碳酸钙,另一个是CaO和水反应生成氢氧化钙,然后和氢氧化钠变质后产生的碳酸钠反应生成的.故该题答案为:CaCO3 Ca(OH)2+Na2CO3=CaCO3↓+2NaOH或Ca(OH)2+CO2=CaCO3↓+H2O.
(2)【猜想】猜想就是提出可能存在的情况,碳酸钠不可能和氢氧化钙共存,再结合题给的条件我们得出的一种可能就是:NaOH和Ca(OH)2
【反思与评价】综合分析甲乙丙三位学生得出的结论,我们看出甲同学向滤液中加稀盐酸产生其他,说明有碳酸钠,丙同学向滤液中加入氢氧化钙后产生沉淀说明存在着碳酸钠,故我们可以得出的结论是滤液中一定存在着碳酸钠. 本题答案为:Na2CO3
要充分证明猜想3也就是验证滤液中含有碳酸钠和氢氧化钠,我们要先验证碳酸钠的存在,然后在排除碳酸钠干扰的条件下验证氢氧化钠的存在,而排除干扰最好就把碳酸钠转化成沉淀或者气体,故我们可以这样做:
(3)经过上面的分析,我们已经判断出有碳酸钠,而由题给条件可知溶解时放热,而在与水接触放出热量的是氢氧化钠,氧化钙与水反应也会放出大量的热,故本题答案应选:②③
(2)【猜想】猜想就是提出可能存在的情况,碳酸钠不可能和氢氧化钙共存,再结合题给的条件我们得出的一种可能就是:NaOH和Ca(OH)2
【反思与评价】综合分析甲乙丙三位学生得出的结论,我们看出甲同学向滤液中加稀盐酸产生其他,说明有碳酸钠,丙同学向滤液中加入氢氧化钙后产生沉淀说明存在着碳酸钠,故我们可以得出的结论是滤液中一定存在着碳酸钠. 本题答案为:Na2CO3
要充分证明猜想3也就是验证滤液中含有碳酸钠和氢氧化钠,我们要先验证碳酸钠的存在,然后在排除碳酸钠干扰的条件下验证氢氧化钠的存在,而排除干扰最好就把碳酸钠转化成沉淀或者气体,故我们可以这样做:
| 实验操作 | 实验现象 | 实验结论及解释 |
| ①取少量滤液C于试管中,加入足量CaCl2溶液 | 有白色沉淀生成 | 猜想③正确 |
| ②过滤,在滤液中滴加无色酚酞试液 | 溶液由无色变成红色 |
点评:本题为实验探究题,做题的关键是抓住题给的资料,并结合所学知识加以解决,记住这类题目中的【查阅资料】部分是非常重要的提示,一定要仔细阅读.

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目



 碱石灰是实验室常用的干燥剂.同学们为确认一瓶久置的“碱石灰”(可能已部分变质或全部变质)样品的成分,进行如下探究.
碱石灰是实验室常用的干燥剂.同学们为确认一瓶久置的“碱石灰”(可能已部分变质或全部变质)样品的成分,进行如下探究.