题目内容
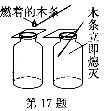
【题目】实验室用加热氯酸钾和二氧化锰混合物的方法制取氧气,小明所在的小组实验后试管破裂了,在对造成试管破裂的原因分析中,你认为正确的个数是![]()
![]()
![]() 酒精灯外焰部分温度太高了
酒精灯外焰部分温度太高了
![]() 氯酸钾与二氧化锰没有混合均匀
氯酸钾与二氧化锰没有混合均匀
![]() 加热前没有预热
加热前没有预热
![]() 试管外壁有水
试管外壁有水
![]() 试管底部与灯芯接触了
试管底部与灯芯接触了
![]() 试管口向上倾斜了
试管口向上倾斜了
![]() 加热后立即用冷水冲冼了试管
加热后立即用冷水冲冼了试管
![]() 用排水法收集氧气结束后先熄灭了酒精灯
用排水法收集氧气结束后先熄灭了酒精灯
A. 8个 B. 7个 C. 6个 D. 5个
【答案】C
【解析】
①酒精灯外焰部分温度太高了不会造成试管破裂,故错误;
②氯酸钾与二氧化锰没有混合均匀不会造成试管破裂,故错误;
③加热前没有预热使试管受热不均,可能会导致试管破裂,故正确;
④试管外壁有水,可能会导致试管破裂,故正确;
⑤试管底部与灯芯接触了使试管受热不均,可能会导致试管破裂,故正确;
⑥试管口向上倾斜了可能会使水冷凝倒流到试管底部,使试管炸裂,故正确;
⑦加热后立即用冷水冲洗了试管,使试管骤冷造成试管破裂,故正确;
⑧用排水法收集氧气结束后先熄灭了酒精灯会使水倒吸入试管内,造成试管破裂,故正确。故选C。

 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案【题目】兴趣小组的同学们在老师的指导下进行实验室制取氧气的实验。
(1)甲同学称取一定质量的高锰酸钾固体放入大试管中,将温度控制在250℃加热制取O2。实验结束时,乙同学发现用排水法收集到的氧气大于理论产量。针对这一现象,进行了如下探究:
[提出猜想]猜想I:反应生成的二氧化锰分解放出氧气;猜想II:反应生成的锰酸钾分解放出氧气;猜想III:_________________
[实验验证]同学们分成两组,分别进行下列实验:第一组同学取一定质量的二氧化锰,在250℃条件下加热一段时间,冷却后测得二氧化锰的质量不变,则猜想______错误;第二组同学取锰酸钾在250℃条件下加热,没有用测定质量的方法得出了猜想II正确的结论。该组同学选择的实验方法是______________。
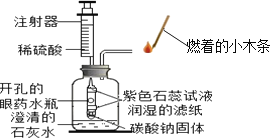
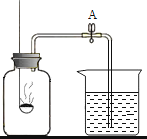
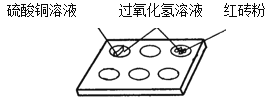
(2)白色点滴板是带有空穴的白色瓷板,可用作微型化学反应。在寻找新催化剂时,将一定量的红砖粉、硫酸铜溶液……分别加入点滴板中,再分别滴入过氧化氢溶液(如图所示),观察到过氧化氢溶液产生气泡的速率加快。据此现象得出结论:红砖粉、硫酸铜溶液等也能做过氧化氢溶液的催化剂。小红认为不正确,
理由一:未探究它们的质量在反应前后是否不变;
理由二:_______________________。
白色点滴板作为反应容器的优点有______________________
(3)通过对催化剂的实验探究,同学们还想探究影响反应速率的其他因素。于是在老师的指导下查阅资料,资料表明:影响反应速率的其他因素还有温度,浓度,物质的纯度和固体的形状大小等。根据查阅的资料同学们设计了实验室用锌与稀硫酸反应制取氢气的实验。反应过程中,用前 10 min 内收集的氢气体积比较反应的快慢。控制其他条件相同,进行下表四组实验,获得数据如下表。
验实号编 | 试剂 | 前 10 min 内产生的氢气体积(mL) | |
不同纯度的锌 | 不同体积和浓度的稀硫酸 | ||
a | 纯锌 | 30 mL 30 % | 564.3 |
b | 含杂质的锌 | 30 mL 30 % | 634.7 |
c | 纯锌 | 30 mL 20 % | 449.3 |
d | 纯锌 | 40 mL 30 % | 602.8 |
① 比较实验 a 和实验 b ,可以得到的结论是________________________。
② 为了研究硫酸浓度对反应快慢的影响,需比较实验_____和实验_____(填编号)。
③ 控制其他条件相同,需控制的条件是__________________(例举一种条件即可)。
通过实验,同学们明白了一个道理,物质的纯度对化学反应速率有很大影响,但是不一定是纯度越大反应速率越快,有时候也会有一些特殊情况。
【题目】下列应用和相应的原理(用化学方程式表示)及基本反应类型正确的是
物质的应用 | 化学方程式 | 反应类型 | |
A | 电解水 | 2H2O2 | 分解反应 |
B | 生石灰中加水能煮熟鸡蛋 | CaO+H2O= Ca(OH)2 | 化合反应 |
C | 金属除锈 | H2SO4+Fe2O3==FeSO4+H2O | 复分解反应 |
D | 比较铜和银的活动性 | Cu + AgNO3 = Cu(NO3)2 + Ag | 置换反应 |
A. A B. B C. C D. D