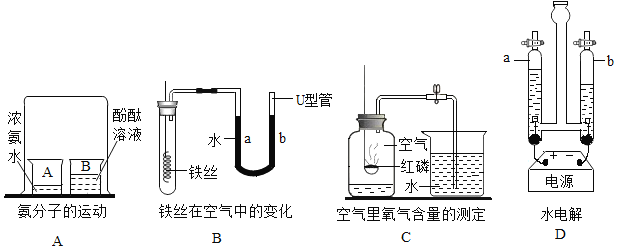
题目内容
【题目】如图为A、B、C、D、E五种微粒的结构示意图,请按要求填空:
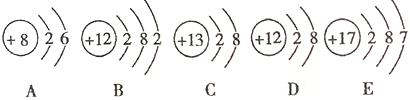
(1)A、B、C、D、E五种粒子中,属于同种元素的是①____________(填序号,下同),属于稳定结构的是②_____________。
(2)E元索的原子在化学变化中容易形成①_________________(填“明离子”或“阳离子”)。元素的化学性质,跟它原子的②_______________关系密切。
(3)由B元素和E元形成的化合物的化学式为_____________________。
【答案】B、D C、D 阴离子 最外层电子数 MgCl2
【解析】
(1)质子数相同的粒子属于同一种元素,由图可知,B、D两种粒子的质子数相同,属于同一种元素;最外层电子数为8(氦为2)属于稳定结构,故属于稳定结构的是C、D;
(2)E原子的最外层电子数为7,大于4个,E元素在化学变化中容易得到电子,形成阴离子;元素的化学性质,跟它原子的最外层电子数关系密切;
(3)由粒子的结构示意图可知,B的质子数是12,属于镁元素,化合价为+2价,E的质子数是17,属于氯元素,化合价为-1价,形成的化合物为氯化镁,化学式为:MgCl2。

【题目】加热条件下.在一个密闭的容器内有如下反应,反应过程中两次测得各物质的质量如表所示:
物质 | P | Q | R | W | ||||
第一次测得的质量/g | 40 | 4 | 3.6 | 4.8 | ||||
第二次测得的质量/g | 待测 | 13 | 12.6 | 10.8 | ||||
| A. | 上述化学反应方程式一定为P | ||||||
| B. | 该反应R与W的质量变化之比为2:3 | ||||||
| C. | 两次测定之间生成W的质量为10.8g | ||||||
| D. | 第二次测得P的质量为16g | ||||||
【题目】善于归纳知识,有利于提高学习能力。下列知识整理的内容不完全正确的一组是
A.化学反应基本类型 | 化学与生活 |
①化合反应 ②分解反应 ③置换反应 ④复分解反应 | ①液氧—可用于火箭的助燃剂 ②人体缺乏碘元素—导致甲状腺肿大 ③鉴别羊毛和合成纤维—点燃后闻气味 ④用洗洁精除去餐具油污—利用乳化作用 |
C.化学实验数据记录 | D.化学中常见的“三” |
①用托盘天平称取7.8g铁粉 ②用50m L量筒量取47.25mL水 ③用pH试纸测得苹果汁的pH为3.2 | ①煤、石油、天然气—三大化石燃料 ②塑料、合成纤维、合成橡胶—三大合成材料 ③分子、原子、离子—构成物质的三种基本粒子 |
A. A B. B C. C D. D
【题目】两位同学帮助老师整理实验室时,在标有“单质”的药柜中发现一瓶失去标签的黑色粉末A,在标有“氧化物”的药柜中发现另一瓶失去标签的黑色粉末B.
(提出问题)这两瓶黑色粉末A和B分别是什么物质?
(猜想)
甲同学:A是铁粉,B是二氧化锰.
乙同学:A是炭粉,B是氧化铜.
(实验探究)
实验步骤 | 实验现象 | 实验结论 |
①取少量A粉末于试管中,加入适量稀硫酸. | 黑色粉末不溶解,没有气体产生. | A粉末一定不是_____. |
②取少量B粉末于试管中,加入适量稀硫酸. | _____,溶液显蓝色. | B粉末是氧化铜. |
(反思与拓展)
(1)将这两种黑色粉末混合加热,观察到黑色粉末逐渐变为红色,澄清石灰水变浑浊.黑色粉末A和B发生反应的化学方程式为_____.
(2)乙同学的猜想正确.