题目内容
【题目】某校化学兴趣小组在“过氧化氢制取氧气的反应中二氧化锰的作用”的探究活动进行了如下探究:
(活动与探究一)实验①:在试管中加入 5mL 5%过氧化氢溶液,把带火星的木条伸入试管, 观察到的现象是______。
实验②:称量 ag 二氧化锰加入上述试管中,把带火星的木条伸入试管,观察到木条复燃了。
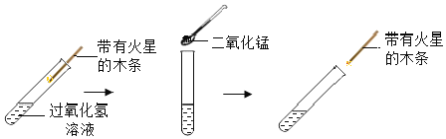
(1)小驰同学得出二氧化锰是这个化学变化中的催化剂。小昌同学认为小驰同学的说法是 不准确的,小昌同学的理由是______。
(活动与探究二)
(2) 用 20mL 5%的过氧化氢溶液进行实验,测定每次收集到 100mL 氧气时所用的时间, 结果如下(其他实验条件如温度等均相同)。
实验次序 | 1 | 2 | 3 | 4 | 5 |
MnO2 用量/g | 0.2 | 0.4 | 0.6 | 0.8 | 1.0 |
所用时间/s | 8 | 5 | 3 | 2 | 2 |
此实验的目的是探究______对过氧化氢分解制氧气反应速率的影响,由上表可以得出的结论是______。收集氧气的方法最好采用______法。该反应的文字表达式______。
(3)请你帮助兴趣小组继续探究催化剂还有哪些其他因素可以影响反应速率(只要求提出 一种影响因素以及相关假设和实验方案)
(假设)_____
(实验方案)_____
【答案】无明显现象(或带火星的小木条不复燃)该实验没有证明二氧化锰的化学性质与质量是否改变催化剂 MnO2 的用量一定范围内,催化剂的质量越大,反应速率越快排水法过氧化氢![]() 水+氧气H2O2分解生成氧气的快慢与二氧化锰颗粒大小有关(合理即可,注意控制变 量)在相同温度下,取两份同体积同浓度的 H2O2 溶液,分别加入质量相同颗粒大 小不同的二氧化锰,测量各收集一瓶相同体积的气体所需要的时间.
水+氧气H2O2分解生成氧气的快慢与二氧化锰颗粒大小有关(合理即可,注意控制变 量)在相同温度下,取两份同体积同浓度的 H2O2 溶液,分别加入质量相同颗粒大 小不同的二氧化锰,测量各收集一瓶相同体积的气体所需要的时间.
【解析】
①过氧化氢在常温条件下反应速度很慢,生成的氧气不足以是带火星的木炭复燃,故填无明显现象(或带火星的小木条不复燃)。
(1)在实验中只能证明二氧化锰能加快反应速度,而其化学性质和质量是否改变没能证明,不能说明二氧化锰是催化剂,故填该实验没有证明二氧化锰的化学性质与质量是否改变。
(2)从表中分析可知每次加入二氧化锰的质量是不同的,故填催化剂 MnO2 的用量;
从图分析可知,加入的二氧化锰的质量越多,生成等量的氧气用的时间越短,故填一定范围内,催化剂的质量越大,反应速率越快;
用排水法收集的气体不会含有其他气体杂质,得到的气体比较纯净,故填排水法;
过氧化氢在二氧化锰作催化剂的条件下反应生成水和氧气,故文字表达式写为过氧化氢![]() 水+氧气。
水+氧气。
(3)二氧化锰的形状也可能影响反应速度,故填在相同温度下,取两份同体积同浓度的 H2O2 溶液,分别加入质量相同颗粒大小不同的二氧化锰,测量各收集一瓶相同体积的气体所需要的时间。

【题目】小明参观某养鱼池,发现农民向养鱼池中撒一种叫做过氧化钙的淡黄色固体用来增加鱼池中含氧量。小明学完氧气的实验室制法,于是他想可否用过氧化钙制取氧气。
(提出问题)过氧化钙可否用于制取氧气?
(查阅资料)部分内容如下:过氧化钙(CaO2)室温下稳定。在300℃时分解生成氧气,可作增氧剂、杀菌剂等。
(猜想与验证)(1)提出猜想:加热过氧化钙可制取氧气。
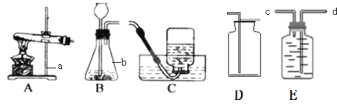
实验装置 | 实验主要过程 |
| ①验装置气密性,操作如下:先将导管伸入液面下,用手紧握试管,观察到有_____,松开手后,有液体进入导管; ②加入过氧化钙,加热,立即收集气体; ③收集满两瓶气体; ④停止加热。熄灭酒精灯前,应_____; ⑤第一瓶用来检验气体。方法是_____; ⑥点燃绑有铁丝的小木条,待小木条快燃尽时伸入到第二瓶气体中,观察到火星四射的现象,请写出该过程中发生反应的文字表达式:_____。 |
(2)验证过程中小明发现实验过程中第五步实验失败了,在老师的帮助下他分析出了原因。你觉得他失败的原因是:_____。
(实验结论)加热过氧化钙可制取氧气。