题目内容
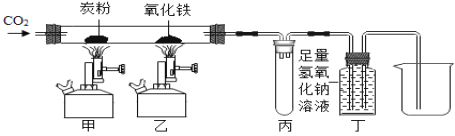
【题目】某研究性学习小组利用下图装置进行一氧化碳还原氧化铁的实验。
回答下列问题:
(1)实验开始时,首先应_____;实验中通入CO2的作用:①排出装置内的空气,②_____(用化学方程式表示)。
(2)写出一氧化碳还原氧化铁的化学反应方程式_____,该反应_____(选填“是”或“否”)置换反应。
(3)丁处试剂瓶中发生的主要反应的化学方程式_____。
(4)对该装置你认为下列说法正确的是_____(选填序号)。
A丙处试管可防止液体倒吸 B该装置的不足之处是未进行尾气处理
(5)当观察到_____(填实验现象),停止加热,待冷却后,用磁铁吸引硬质玻璃管中的黑色粉末,黑色粉末被吸起。小军同学说,该黑色粉末是铁。小明说,该黑色粉末不一定是铁。于是,他们对生成的黑色粉末进行探究。
查阅资料:①CO还原Fe2O3的产物与反应温度有关。
②Fe3O4为黑色粉末,能与盐酸反应,含有Fe3+的盐溶液遇到KSCN(硫氰化钾)溶液时变成红色,Fe(OH)2是一种白色沉淀,在空气中易被氧气氧化。
进行实验:
实验操作 | 现象 |
步骤一:取黑色粉末加入盐酸 | 溶解,无气泡,溶液呈浅黄绿色 |
步骤二:取步骤一所得溶液,滴加KSCN溶液 | 溶液变红 |
步骤二:再取步骤一所得溶液,加入足量的NaOH溶液 | 有红褐色沉淀生成,同时还有少量的白色沉淀生成,但最终白色沉淀都变成了红褐色沉淀 |
实验结论:①黑色粉末是_____(填名称)。
②写出黑色粉末与盐酸反应的化学方程式_____。
【答案】检查装置的气密性 CO2+C![]() 2CO 3CO+Fe2O3
2CO 3CO+Fe2O3![]() 2Fe+3CO2 否 CO2+2NaOH=Na2CO3+H2O A 乙处红色固体全部变成黑色时 四氧化三铁 Fe3O4+8HCl=FeCl2+2FeCl3+4H2O
2Fe+3CO2 否 CO2+2NaOH=Na2CO3+H2O A 乙处红色固体全部变成黑色时 四氧化三铁 Fe3O4+8HCl=FeCl2+2FeCl3+4H2O
【解析】
(1)实验开始时,首先要检查装置的气密性,实验中通入二氧化碳的作用,一是排出装置内空气,二是与炭粉反应生成一氧化碳,所以填:检查装置的气密性 CO2+C![]() 2CO;
2CO;
(2)一氧化碳与氧化铁反应时,生成铁和二氧化碳,该反应不是置换反应,所以填:3CO+Fe2O3![]() 2Fe+3CO2 否
2Fe+3CO2 否
(3)丁处是生成的二氧化碳或原来未参加反应的二氧化碳与氢氧化钠反应生成碳酸钠和水,所以填:CO2+2NaOH=Na2CO3+H2O
(4)对该装置:反应后若停止加热则丁中的液体会被倒吸到丙处,不会被吸入热的试管中,所以丙处试管可防止液体倒吸,由于丁装置可吸收二氧化碳,同时可将一氧化碳贮存在瓶内,所以不需要加尾气处理装置。所以填:A
(5)当观察到乙处的红色固体全部变成黑色时,说明反应结束,此时停止加热。
根据现象加盐酸无气泡,说明没有铁,加KSCN溶液,变红则说明有Fe3+,另取溶液加氢氧化钠溶液有白色沉淀生成,则说明有Fe2+,所以此黑色粉末是四氧化三铁,四氧化三铁与盐酸反应时生成氯化铁、氯化亚铁和水,所以填:四氧化三铁 Fe3O4+8HCl=FeCl2+2FeCl3+4H2O