题目内容
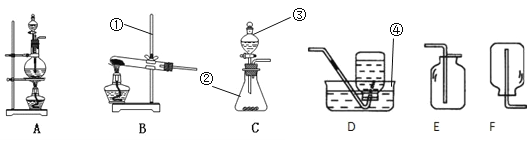
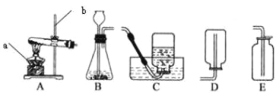
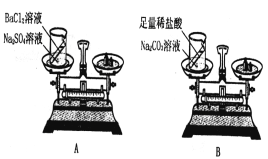
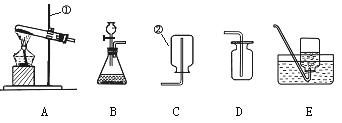
【题目】根据下列装置图回答问题(装置图用序号填空)。
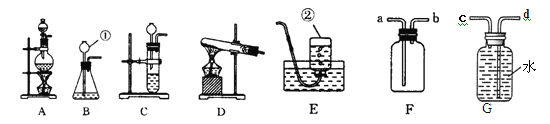
(1)写出编号①和②仪器的名称:① ②
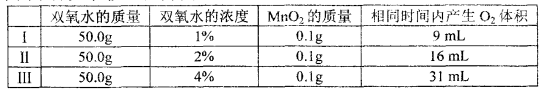
(2)实验室加热KMnO4制O2时,应选用 做气体发生装置。
反应的化学方程式为; ,可用装置E收集氧气的原因是 。实验室制取H2时,应选用 做气体发生装置。已知MnO2固体和浓盐酸混合共热可制得氯气(Cl2),则应选用 做气体发生装置。
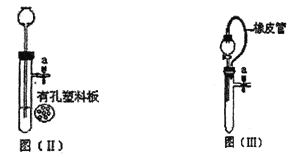
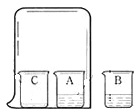
(3)有一名同学欲用F装置收集H2,则H2应从导管口 通入。另一同学欲用G装置收集氧气,则O2应从导管口 通入。
(4)实验室若用B装置来制取二氧化碳时,往长颈漏斗中应加入 ,反应的化学方程式为 ,若用F来收集二氧化碳,二氧化碳应从 进入(选“a”或“b”) 。检验二氧化碳的方法是 ,其反应的化学方程式 。
【答案】(1)①长颈漏斗 ②集气瓶
(2)D 2KMnO4 △K2MnO4 + MnO2 + O2↑ 氧气不易溶于水 B或C A
(3)b c (4)稀盐酸 CaCO3+2HCl==CaCl2+H2O+CO2↑
a 注入澄清石灰水 石灰水变浑浊,是二氧化碳 CO2 +Ca(OH)2 ==CaCO3↓+ H20
【解析】
试题分析:(1)常见仪器的识记
(2)气体发生装置的选择依据:反应物的状态和反应条件,加热KMnO4制O2,属于固体与固体反应且需加热,故应选用发生装置D,反应的化学方程式为:2KMnO4 △K2MnO4 + MnO2 + O2↑,可用装置E(即排水法)收集氧气的原因是:氧气不易溶于水,实验室制取H2,是利用固体锌和液体稀硫酸反应,故气体发生装置选择B或C, 而MnO2固体和浓盐酸混合共热可制得氯气(Cl2),则应选用气体发生装置A
(3)用F装置收集H2,因为氢气的密度比空气小,故H2应从短管进,即导管口b通入,而用G装置(里面充满了水,即排水法)收集氧气,气体固定从短管进气,故O2应从导管口c通入
(4)用B装置来制取二氧化碳时,往长颈漏斗中应加入稀盐酸,反应的化学方程式为:CaCO3+2HCl==CaCl2+H2O+CO2↑,用F来收集二氧化碳,因为二氧化碳的密度比空气大,故二氧化碳应从短管,即a端进入,检验二氧化碳的方法是:注入澄清石灰水 石灰水变浑浊,是二氧化碳,反应的化学方程式:CO2 +Ca(OH)2 ==CaCO3↓+ H20

【题目】气体分子之间的间距比较大,所以容易被压缩。某同学想:当气体的质量一定时,气体压缩,体积减小的时候,气体压强将会怎样变化呢?
(1)他提出了两个猜想:
猜想A:一定质量的气体,压缩体积,压强减小;
猜想B:一定质量的气体,压缩体积,压强增大。
但经仔细一想,该同学马上否定了自己的猜想A。
你认为该同学否定猜想A的理由是: 。
(2)进一步思考:压强和体积的变化满足什么样的关系呢?
他找来一个注射器和一个气压计,在注射器里边封了30ml空气(不计注射器活塞重力和摩擦,注射器完全密封,大气压强P0=1.0×105Pa)。
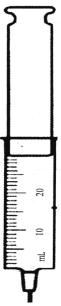
查阅资料得知:气体被压缩的时候,内能增加,温度上升也引起压强的变化。所以在下面的实验过程中要注意控制 相同。
以下是该同学实验时记录的数据:
实验次数 | 1 | 2 | 3 | 4 | 5 |
体积(ml) | 30 | 25 | 20 | 15 | 10 |
压强(×105pa) | 1 | 1.2 | 1.5 | V | 3 |
(3)表格中V= ;
(4)分析以上数据,写出一定质量气体的体积和压强定量关系 。