题目内容
【题目】某工厂的废水中含有MgSO4和FeCl3,技术人员逐渐加入NaOH溶液调节废水的pH,先后分离出两种沉淀,并通过系列处理得到有价值的产品,操作流程如图所示。
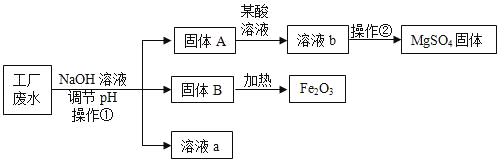
(1)NaOH溶液的pH_____7(填“<”“=”或“>”):操作①的名称是_____,实验室中此操作要用到的玻璃仪器有玻璃棒、烧杯、_____。
(2)固体A与某酸反应的化学方程式为_____,操作②时,当_____即可停止加热。
(3)固体B加热的产物是两种常见氧化物,则另一种氧化物的化学式为_____。
(4)溶液a除了可能含有NaOH外,还一定含有的溶质是_____(填化学式)。
【答案】> 过滤 漏斗 Mg(OH)2+H2SO4=MgSO4+2H2O 剩余少量水(或析出大量晶体) H2O NaCl、Na2SO4
【解析】
(1)NaOH溶液为碱性溶液,pH>7;操作①实现固液分离,为过滤,实验室中此操作要用到的玻璃仪器有玻璃棒、烧杯、漏斗。故填:>;过滤;漏斗
(2)固体A与某酸反应,由于生成硫酸镁,所以是和硫酸反应,所以对应的反应为氢氧化镁和硫酸反应生成硫酸镁和水,对应的化学方程式为 Mg(OH)2+H2SO4=MgSO4+2H2O.操作②时,当 剩余少量水(或析出大量晶体)即可停止加热。故填:Mg(OH)2+H2SO4=MgSO4+2H2O;剩余少量水(或析出大量晶体);
(3)固体B为氢氧化铁,加热的产物是两种常见氧化物,分别为氧化铁和水,所以另一种氧化物的化学式为 H2O。故填:H2O
(4)溶液a除了可能含有剩余的NaOH外,还一定含有的溶质是生成的 NaCl和Na2SO4。故填:NaCl、Na2SO4

练习册系列答案
相关题目