题目内容
【题目】实验技能训练中,小亮同学向氧化铜和稀硫酸充分反应后的废液中加入一定量的氢氧化钠溶液,发现无明显现象。小亮同学在老师的指导下对反应后的废液进行了实验:他分别取50g废液,并向其中逐渐加入等浓度的氢氧化钠溶液,三组实验的数据与其中一组的图象如下:
实验组数 | 第一组 | 第二组 | 第三组 |
加入氢氧化钠溶液质量/g | 50 | 100 | 80 |
产生沉淀的质量/g | 0.98 | 2.94 | 2.94 |
请根据以上信息回答下列问题:所得
(1)废液中的溶质有_____(填化学式)。
(2)计算废液中硫酸铜的溶质质量分数。_____(写出计算过程)
(3)若三组数据中,只有某一组加入的氢氧化钠溶液与废液恰好完全反应,则该实验为第_____组,下图中a的数值为_____。
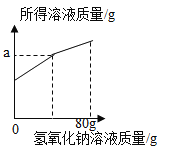
【答案】H2SO4、CuSO4 9.6% 三 127.06
【解析】
由于开始加入的50g氢氧化钠溶液得到的沉淀质量小于第二次加入的,所以应该是废液中的溶质有 H2SO4、CuSO4。
第一阶段是和硫酸反应,第二阶段是和硫酸铜反应
设废液中硫酸铜的溶质质量分数为x
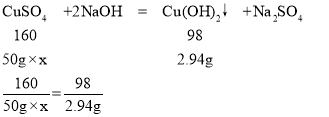
x=9.6%
只有第三组是恰好完全反应,右图中a的数值为 50g+80g-2.94g=127.06g
故答案为:
(1)H2SO4、CuSO4。
(2)9.6%。
(3)三; 127.06。

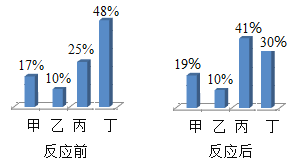
【题目】某研究小组为探究“影响铁制品锈蚀快慢的因素”,取同浓度的氨水和稀醋酸用下图装置完成表中实验,回答下列问题。
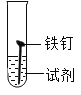
实验序号 | ① | ② | ③ | ④ |
实验温度/℃ | 25 | 25 | 70 | 70 |
试剂 | 稀氨水 | 稀醋酸 | 稀氨水 | 稀醋酸 |
出现铁锈所需时间 | 1天未见锈蚀 | 5分钟 | 1天未见锈蚀 | 1分钟 |
(1)实验②和④可探究_____因素对铁制品锈蚀快慢的影响;欲探究试剂酸碱性对铁制品锈蚀快慢的影响,应选择的实验是_____(填实验序号)。
(2)根据表中实验现象得出的结论是_____(写出一条即可)。
该研究小组中的小金同学提出要探究铁制品锈蚀的条件,并进行如下实验:
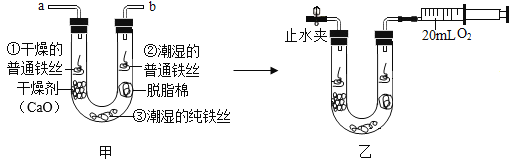
步骤1:利用图甲所示装置,将干燥的氧气从导管a通入U形管(装置气密性良好,药品如图所示);待U形管内充满氧气后,在导管b处连接一活塞推至底部的注射器,收集20ml氧气后在导管a处连接乳胶管并用止水夹夹紧,如图乙所示。
步骤2:一段时间后,观察U形管内的铁丝,其现象如图所示。
观察对象 | 现象 |
①干燥的普通铁丝 | 没有明显变化 |
②潮湿的普通铁丝 | 较多红褐色锈斑 |
③潮湿的纯铁丝 | 没有明显变化 |
(3)铁制品锈蚀的条件之一是需要氧,在此实验中能支持此条件的现象是_____。
(4)通过对比①②的实验现象,可以得出铁制品锈蚀与_____有关;通过对比_____的实验现象还可得出铁制品锈蚀与金属的内部结构有关。