题目内容
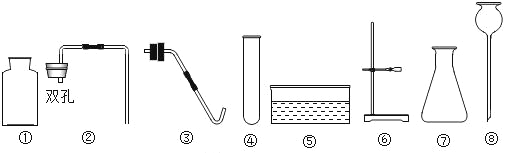
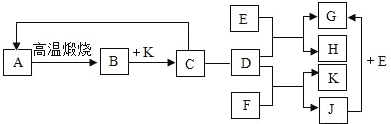
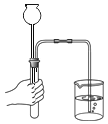
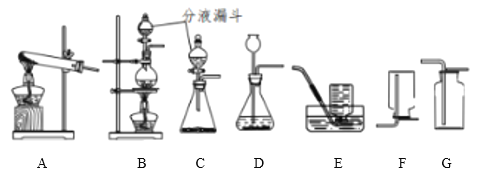
【题目】分液漏斗是化学实验室制备气体的一种常用的仪器,可用于滴加液体或分离互不相溶的两种液体,实验室部分装置如A-G所示
(实验探究)
(1)高锰酸钾、过氧化氢和氯酸钾都可制取氧气,下列有关这三种物质说法正确的是(_____)
A.它们都含有三种元素,其中一种是氧元素
B.它们制取氧气的反应都是分解反应
C.它们制取氧气时均需用二氧化锰作催化剂
(2)请写出实验室加热KMnO4固体制取O2的化学方程式:
_______________________________________________________;
此时应采用的发生装置为_________________;实验室采用加热NH4Cl溶液与NaNO2溶液可制取氮气,此反应采用的发生装置为___________________ 。
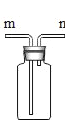
(3)请写出实验室制取CO2的化学方程式____________________________________,装置C、D均应可以用来制取CO2,与D相比较,C主要的优点是 _______________________________,收集CO2应选择的装置是______________。
(4)通过查阅资料可知:常温下将浓氨水加入到生石灰固体中可制取氨气,此反应采用的发生装置为________,将制取得到的氨气通入无色的酚酞溶液现象为_________________。
(5)关于装置C和D的下列说法正确的是__________________ (双项选择)
A.装置C发生反应时,分液漏斗下端必须浸没在液体中
B.装置D发生反应时,长颈漏斗下端必须浸没在液体中
C.装置C和D的气密性检查的操作方法相同
D.装置C和D均可用于制取一定量的H2
【答案】B 2KMnO4![]() K2MnO4+ MnO2+O2↑ A B CaCO3+2HCl=CaCl2+H2O+CO2↑ 既可以控制反应的速率,又能随时控制反应的发生和停止,节约药品 G C 溶液变红 BD
K2MnO4+ MnO2+O2↑ A B CaCO3+2HCl=CaCl2+H2O+CO2↑ 既可以控制反应的速率,又能随时控制反应的发生和停止,节约药品 G C 溶液变红 BD
【解析】
(1)
A、过氧化氢含有2种元素,高锰酸钾和氯酸钾含有三种元素,它们都含有氧元素,故选项不正确;
B、过氧化氢分解生成水和氧气,高锰酸钾分解生成锰酸钾和二氧化锰和氧气,氯酸钾分解生成氯化钾和氧气,都是分解反应,故选项正确;
C、过氧化氢和氯酸钾分解制氧气需要二氧化锰催化,高锰酸钾制氧气不需要二氧化锰催化,故选项不正确;故填B;
(2)高锰酸钾分解生成锰酸钾和二氧化锰和氧气,方程式故填2KMnO4![]() K2MnO4+ MnO2+O2↑; 高锰酸钾是固体,反应需要加热,发生装置故填A;实验室采用加热NH4Cl溶液与NaNO2溶液可制取氮气,反应物是液体,条件是加热,此反应采用的发生装置应选B,故填B;
K2MnO4+ MnO2+O2↑; 高锰酸钾是固体,反应需要加热,发生装置故填A;实验室采用加热NH4Cl溶液与NaNO2溶液可制取氮气,反应物是液体,条件是加热,此反应采用的发生装置应选B,故填B;
(3)实验室用大理石或石灰石和稀盐酸反应制取CO2,同时还生成氯化钙和水,化学方程式故填CaCO3+2HCl=CaCl2+H2O+CO2↑;装置C中使用了分液漏斗,通过控制分液漏斗的活塞,既可以控制反应的速率,又能随时控制反应的发生和停止,还节约了药品,而装置D中使用长颈漏斗便于随时添加液体,故填既可以控制反应的速率,又能随时控制反应的发生和停止,节约药品;二氧化碳可溶于水且与水反应,不能用排水法收集,相同条件下二氧化碳密度比空气大,且不于空气中各成分反应,可以采用向上排空气法收集,收集CO2应选择的装置故填G;
(4)常温下将浓氨水加入到生石灰固体中可制取氨气,可知反应物是固体和液体,反应条件是常温,选择固液混合不加热型,浓氨水具有挥发性,极易挥发出氨气,发生装置故填C;生成的氨气溶于水得到的氨水显碱性,能使无色的酚酞溶液变红,故填溶液变红;
(5)
A、分液漏斗下端有活塞,装置C发生反应时,打开下端活塞即可,分液漏斗下端不需要浸没在液体中,故选项不正确;
B、装置D发生反应时,长颈漏斗下端必须浸没在液体中,构成封闭体系,故选项正确;
C、装置C常用加热法检查气密性,装置D常用注水法检查气密性,操作方法不相同,故选项不正确;
D、实验室常用锌粒和稀硫酸在常温下反应制氢气,反应物是固液混合不加热型,可以采用装置C或D,故选项正确;故填BD。

 名校课堂系列答案
名校课堂系列答案【题目】请根据下列装置回答问题。
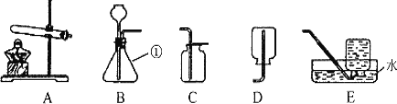
(1)写出图中标号①的仪器名称_____。
(2)实验室用高锰酸钾制氧气的化学方程式为_____, 选择的发生装置是_____(填装置序号,下同),若要收集一瓶供铁丝燃烧实验用的氧气,最适宜选择收集装置是_____。
(3)小组同学为了研究用向上排空气法和排水法收集的氧气浓度是否有差异,做了如下实验:加热高锰酸钾固体,分别用两种方法各收集三瓶氧气,并使用传感器测定收集到的氧气浓度,数据见表。
收集方法 | 向上排空气法 | 排水法 | ||||
氧气浓度/% | 79.6 | 79.7 | 79.9 | 90.0 | 89.8 | 89.3 |
氧气平均浓度/% | 79.7 | 89.7 | ||||
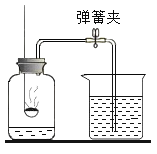
① 用向上排空气法收集氧气时,以能使放置在集气瓶瓶口的带火星木条复燃为氧气集满的标准;用排水法收集氧气时,以观察到_____为氧气集满的标准;
② 向上排空气法收集到的氧气浓度只有 80%左右,下列说法错误的是______填字母序号)。
a.氧气的密度略大于空气的密度,无法将空气排尽
b.加热高锰酸钾固体产生氧气的浓度只有 80%左右
c.当观察到带火星木条复燃时,集气瓶内还有剩余空气