题目内容
【题目】废旧电路板中主要含有塑料、铜和锡(Sn)等,为实现对其中锡的绿色回收,某工艺流程如下:
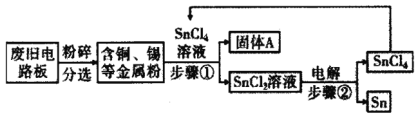
已知:Sn十SnCl2===2SnCl2
(1)SnCl2中锡元素的化合价是___________。
(2)步骤①的操作是_____,固体A中一定含有的金属元素是_____。
(3)写出步骤②发生反应的化学方程式______________。
(4)相比于直接焚烧废旧电路板回收金属,该工艺的主要优点是__________(回答一点即可)
【答案】+2 过滤 Cu 2SnCl2![]() Sn+SnCl4 避免焚烧塑料产生污染,更加环保
Sn+SnCl4 避免焚烧塑料产生污染,更加环保
【解析】
(1)SnCl2中,氯元素的化合价为﹣1,根据化合物中各元素的化合价为零可知,锡元素的化合价为+2;
(2)步骤①是固体和液体分离,所以操作是过滤,在金属活动顺序表中铜排在锡之后,铜的金属活动性比锡的弱,所以加入铜不能与SnCl4反应,所以固体A中一定含有的金属元素是Cu;
(3)步骤②中SnCl2在通电的条件下分解生成SnCl4和Sn,化学方程式为:2SnCl2![]() SnCl4+Sn;
SnCl4+Sn;
(4)相比于直接焚烧废旧电路板回收金属,该工艺主要优点是避免焚烧塑料产生污染,更加环保。

【题目】某化学兴趣小组对一包干燥的红色粉末组成进行探究。请你参与并回答问题。
(教师提醒)它由Cu 、Fe2O3两种固体中的一种或两种组成。
(提出猜想)红色粉末可能的组成,
猜想①:红色粉末是Cu; 猜想②:红色粉末是Fe2O3;
猜想③:红色粉末是Cu 和Fe2O3的混合物
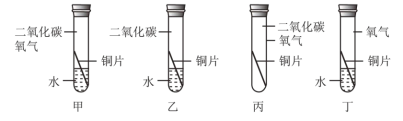
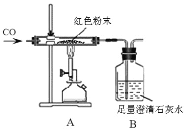
(实验探究)同学们为确定红色粉末的组成,称取该粉末5.0g装入硬质玻璃管中,按右下图在通风橱中进行实验。
反应前后称量相关装置和物质的总质量,其数据如下表:
反应前 | 反应后 |
玻璃管和红色粉末的总质量为37.3 g | 玻璃管和固体物质的总质量为36.1 g |
(1)A装置中发生反应的化学方程式_______,玻璃管中应该观察到的现象是_________
(2)小蒋同学初步分析表中的数据后,马上得出猜想_______(填“①”“②”“③”)肯定不正确,理由是_______________。
(3)有同学认为为了防止烧杯中液体倒吸,本实验停止加热前应先断开A和B的连接,但小明认为不需要,理由是_________________
(反思评价)(4)实验后小组内有同学指出:上图装置未进行尾气的处理。于是有同学设计了用如图装置代替原装置,则C装置的作用有___________________(至少答两点)。

【题目】某化学小组同学做镁条在空气中燃烧实验时,发现生成物中还有少量黑色固体,针对这一现象及相关问题,他们开展了如下探究,请仔细阅读并参与他们的探究之旅。
(探究目的)探究黑色固体是镁与空气中什么物质反应产生的?
(查阅资料)1.稀有气体一般与其他物质反应 2.光亮的镁条与水反应,表面会生成白色固体。
(分析猜想)分析空气中各种成分,进行猜想:
(1)猜想①是氧气 猜想②是氮气 猜想③是__________________
(实验一)镁带与氧气的反应
(一)甲同学探究了影响过氧化氢制取氧气速度的某种因素,进行了三次实验并记录各收集相同体积氧气所需要的时间如下表
实验 | 过氧化氢的浓度 | 过氧化氢溶液质量/g | 二氧化锰质量/g | 收集时间/s |
1 | 10% | 20 | 40 | |
2 | 15% | 20 | 1 | 20 |
3 | 20% | X | 1 | 12 |
(2)第 3 次实验中,X 的值应为_____
(3)实验结论:在相同条件下,___________________过氧化氢分解得越快。
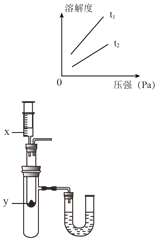
(二)乙同学在量筒中盛满水,倒置于水槽中,通过分液漏斗把 20mL 某浓度的过氧化氢溶液加入锥形瓶中,记录量筒中气体的体积(如图 )。数据如下表:
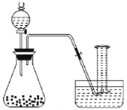
时间/min | 1 | 3 | 5 | 7 | 9 | 10 |
量筒读数/mL | 60.0 | 82.0 | 88 | 89.5 | 90 | 90 |
(4)请根据以上过程和实验数据综合分析,最终生成氧气的体积是_____mL
(5)请在下面坐标图中绘制出 0~10 min 生成氧气体积随时间变化的曲线_____________。
(三)燃烧镁带,观察现象
将镁带打磨光亮,点燃伸入盛满氧气的集气瓶中,产生大量白烟,生成白色固体。实验结论:镁与氧气反应生成白色的氧化镁
(实验二)镁带与氮气反应
(一)收集氮气
(二)燃烧镁带,观察现象
将镁带打磨光亮,点燃伸入盛满氮气的集气瓶中,瓶内壁附着一层淡黄色的固体。
(6)实验结论:镁与氮气在点燃条件下发生化合反应生成淡黄色的氮化镁(Mg3N2) 该反应的化学方程式是________
(探究结论 1)(7)综上分析,关于镁在空气中燃烧产生黑色固体的猜想是猜想__________(填序号)成立。
(探究结论 2)(8)如果用足量的镁代替红磷进行空气组成实验,实验测得氧气的体积分数比实际值______(填“偏大”或“偏小”)
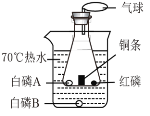
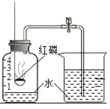
(实验回顾)实验室常用红磷燃烧的方法测定空气中氧气含量(如图),由于红磷需要在瓶外点燃再伸入瓶内,常常带来污染以及误差。
(实验改进)同学们选择了着火点更低的白磷,并对装置图做了改进(如图)。主要操作是:在实际容积为 180mL 的集气瓶里,先装进 50mL 的水,再按图连好仪器,按下热的玻璃棒,白磷立即被点燃。
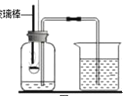
(9)白磷从燃烧到熄灭冷却的过程中,瓶内水面的变化是______________
(10)若实验中无误差,最终集气瓶中水的体积为__________________mL
(11)集气瓶里预先装置的 50mL 水的作用,其一是为了加快集气瓶的冷却速度,其二则主要是_____________
(实验与交流)
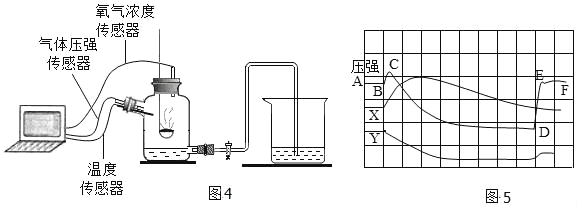
(12)为了帮助同学们更好地理解空气中氧气含量的实验原理,老师利用传感器技术定时测定了实验装置(图 4)内的压强、温度和氧气浓度,三条曲线变化趋势如图 5 所示。Y 曲线表示的是_______________(填“温度”或“氧气浓度”或“压强”)变化趋势;X 曲线中 CD 段上升的原因是___________
【题目】实验室用如图装置进行碳酸钠的性质实验,烧杯A中是澄清石灰水并滴加了酚酞,C中是石灰乳.实验开始前,称取10.6g纯碱置于B中,关闭开关K1打开K2,并加入一定量的稀硫酸.
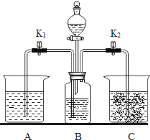
①烧杯C中并没有明显现象,为了证明B中的确产生了CO2,现将C中液体进行固液分离,该分离操作除烧杯外,还需用到的玻璃仪器有_____ (写名称).过滤后滤液能使酚酞试液变红,则滤液中的主要溶质是_____,该现象_________ (填写“能”或“不能”)说明产生了CO2.
②上述过滤后的滤渣可能存在Ca(OH)2和CaCO3.某同学为证明该两种物质同时存在,在一支试管中取少量样品,经过两个步骤完成了检验.若所有检验实验均在该支试管中进行,请完成实验报告:
实验步骤 | 所用的试剂或检验方法 | 结 论 |
步骤一 | _________ | 证明______存在 |
步骤二 | _________ | 证明_______存在 |
③实验一段时间后,关闭开关K2打开K1,见到B中液体将会压入到烧杯A中,实验中可能见到不同的现象,请完成下表:
预测的反应现象 | B中反应后,溶液中溶质的化学式 | 烧杯A中发生的主要反应的化学方程式 |
A中溶液产生大量的白色沉淀产生,红色不褪去. | _________ | _______________ |
A中溶液并没有大量的白色沉淀产生,红色褪去. | _____________ | ________________ |