题目内容
兴趣小组同学为了探究实验室中久置的氢氧化钙固体的成分,进行了有关实验.请你与他们一起完成以下探究活动:
猜想Ⅰ.全部是Ca(OH)2; 猜想Ⅱ.全部是CaCO3
猜想Ⅲ. .
小明同学取固体样品于试管中,加少量水,振荡,静置,发现有白色沉淀出现,他认为氢氧化钙已发生变质.小红同学提出质疑,认为小明的实验不足以说明氢氧化钙已变质.其理由是 .
小雯同学设计了如下实验方案: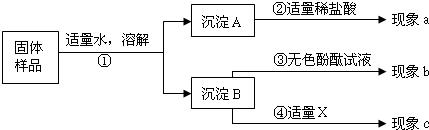
(1)若现象a为有气泡产生,说明沉淀A中含有的物质名称是 .
(2)若X是CO2气体,现象c无白色沉淀,则说明样品中 (填“有”或“没有”)Ca(OH)2.综合(1)和(2)的结论,得出猜想 成立.
(3)若X是Na2CO3溶液,猜想Ⅲ成立的实验现象是:现象a为有 产生,现象b为无色酚酞试液 色,现象c为 .产生现象c的反应的化学方程式为 .
若(3)反应后的废液直接倒入下水道,会污染环境.小雯同学用适量稀硫酸处理废液,但不知是否恰好完全中和.于是,小强同学设计了如下实验方案来验证:
①有同学提出质疑,认为上述实验方案不足以证明处理后的废液一定显中性,理由是: .为此,还需要从以下选项中选择一种试剂再进行实验验证,其中可行的是 (填字母).
A.石蕊溶液 B.Ba(NO3)2溶液 C.锌粒 D.生锈的铁钉
②久置的氢氧化钙变质的化学方程式是 .
猜想Ⅰ.全部是Ca(OH)2; 猜想Ⅱ.全部是CaCO3
猜想Ⅲ.
小明同学取固体样品于试管中,加少量水,振荡,静置,发现有白色沉淀出现,他认为氢氧化钙已发生变质.小红同学提出质疑,认为小明的实验不足以说明氢氧化钙已变质.其理由是
小雯同学设计了如下实验方案:

(1)若现象a为有气泡产生,说明沉淀A中含有的物质名称是
(2)若X是CO2气体,现象c无白色沉淀,则说明样品中
(3)若X是Na2CO3溶液,猜想Ⅲ成立的实验现象是:现象a为有
若(3)反应后的废液直接倒入下水道,会污染环境.小雯同学用适量稀硫酸处理废液,但不知是否恰好完全中和.于是,小强同学设计了如下实验方案来验证:
| 实验步骤 | 实验现象 | 结论 |
| 取少量处理后的废液于试管中,滴入无色酚酞溶液. | 若 |
处理后的废液仍然显碱性 |
| 若没有明显现象 | 处理后的废液显中性 |
A.石蕊溶液 B.Ba(NO3)2溶液 C.锌粒 D.生锈的铁钉
②久置的氢氧化钙变质的化学方程式是
分析:【对固体猜想】根据变之前后的物质的组合进行分析;
【实验】根据氢氧化钙的溶解度较小进行分析;
(1)根据酸和碳酸盐反应会生成二氧化碳气体进行分析;
(2)根据二氧化碳和氢氧化钙会生成碳酸钙沉淀进行分析;
(3)根据碳酸钙和盐酸会生成气体,氢氧化钙显碱性,氢氧化钙和碳酸钠会生成沉淀进行分析;
根据酚酞遇碱变红色进行分析;
①根据酚酞遇酸性和中性都不变色进行分析;
②根据二氧化碳和氢氧化钙会生成碳酸钙沉淀进行分析.
【实验】根据氢氧化钙的溶解度较小进行分析;
(1)根据酸和碳酸盐反应会生成二氧化碳气体进行分析;
(2)根据二氧化碳和氢氧化钙会生成碳酸钙沉淀进行分析;
(3)根据碳酸钙和盐酸会生成气体,氢氧化钙显碱性,氢氧化钙和碳酸钠会生成沉淀进行分析;
根据酚酞遇碱变红色进行分析;
①根据酚酞遇酸性和中性都不变色进行分析;
②根据二氧化碳和氢氧化钙会生成碳酸钙沉淀进行分析.
解答:解:【对固体猜想】氢氧化钙也可能是部分变质,故答案为:是Ca(OH)2和CaCO3的混合物;
【实验】氢氧化钙在水中的溶解度较小,氢氧化钙较多时,也会出现白色沉淀,故答案为:氢氧化钙微溶于水,当达到饱和状态时,也会出现白色沉淀;
【判断】(1)盐酸和碳酸钙会生成二氧化碳气体,故答案为:碳酸钙
(2)二氧化碳和氢氧化钙会生成白色的碳酸钙沉淀,故答案为:没有Ⅱ;
(3)猜想三是碳酸钙和氢氧化钙,碳酸钙和盐酸会生成二氧化碳气体,氢氧化钙会使酚酞变红色,氢氧化钙和碳酸钠会生成碳酸钙沉淀和氢氧化钠,故答案为:气泡 变红 产生白色沉淀 Ca(OH)2+Na2CO3═CaCO3↓+2NaOH
【拓展】酚酞遇碱性溶液会变红色,
【反思】①中性的溶液或酸性液体都不会使酚酞变色,故答案为:若溶液显酸性时,无色酚酞溶液也不变色;
石蕊遇酸变红色,锌和酸会生成气体,氧化铁和酸反应,溶液会变成黄色,故答案为:ACD;
②氢氧化钙和二氧化碳反应会生成碳酸钙和水,故答案为:Ca(OH)2+CO2═CaCO3↓+H2O
【实验】氢氧化钙在水中的溶解度较小,氢氧化钙较多时,也会出现白色沉淀,故答案为:氢氧化钙微溶于水,当达到饱和状态时,也会出现白色沉淀;
【判断】(1)盐酸和碳酸钙会生成二氧化碳气体,故答案为:碳酸钙
(2)二氧化碳和氢氧化钙会生成白色的碳酸钙沉淀,故答案为:没有Ⅱ;
(3)猜想三是碳酸钙和氢氧化钙,碳酸钙和盐酸会生成二氧化碳气体,氢氧化钙会使酚酞变红色,氢氧化钙和碳酸钠会生成碳酸钙沉淀和氢氧化钠,故答案为:气泡 变红 产生白色沉淀 Ca(OH)2+Na2CO3═CaCO3↓+2NaOH
【拓展】酚酞遇碱性溶液会变红色,
| 实验步骤 | 实验现象 | 结论 |
| 无色酚酞溶液变红色 | ||
石蕊遇酸变红色,锌和酸会生成气体,氧化铁和酸反应,溶液会变成黄色,故答案为:ACD;
②氢氧化钙和二氧化碳反应会生成碳酸钙和水,故答案为:Ca(OH)2+CO2═CaCO3↓+H2O
点评:在解此类题时,首先分析题中考查的问题,然后结合学过的知识和题中的知识进行分析解答.

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目

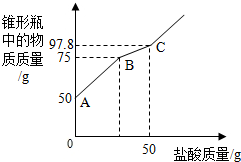 兴趣小组同学为了探究实验室中久置的氢氧化钠固体的成分,进行了有关实验.请你与他们一起完成以下探究活动:
兴趣小组同学为了探究实验室中久置的氢氧化钠固体的成分,进行了有关实验.请你与他们一起完成以下探究活动: