题目内容
【题目】将一定质量的某金属R放入l00g 14.6%稀盐酸中,恰好完全反应。实验测得R的氯化物中氯元素含量为52.2%,计算:
(1)反应生成的气体质量是多少?
(2)金属R的质量是多少克?
【答案】(1)0.4g(2)13g
【解析】
(1)金属与盐酸刚好完全反应,则盐酸中的氢元素全部转变为氢气,即氢气的质量等于盐酸中氢元素的质量。l00g 14.6%稀盐酸中氢元素的质量为:![]() ×100g×14.6%=0.4g;
×100g×14.6%=0.4g;
(2)反应物盐酸中氯元素的质量为![]() ×100g×14.6%,等于生成的R的氯化物中氯元素的质量,因为测得R的氯化物中氯元素含量为52.2%,所以R的氯化物的质量为
×100g×14.6%,等于生成的R的氯化物中氯元素的质量,因为测得R的氯化物中氯元素含量为52.2%,所以R的氯化物的质量为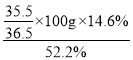 ≈27.2g,所以R的质量为27.2g+0.4g-14.6g=13g.
≈27.2g,所以R的质量为27.2g+0.4g-14.6g=13g.

练习册系列答案
相关题目