题目内容
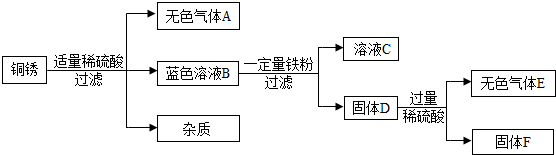
(2013?盐城一模)A、B、C、D、E、F是初中化学内容所涉及到的物质,其中A、B是氧化物,在一定条件下,它们的转化关系如图所示:

根据图推断:
(1)F中金属元素的化合价为
(2)D物质在氧气中燃烧,也能生成B,则B的化学式为
(3)写出D与稀硫酸反应的化学方程式
(4)物质A的一种用途

根据图推断:
(1)F中金属元素的化合价为
+2价
+2价
.(2)D物质在氧气中燃烧,也能生成B,则B的化学式为
Fe3O4
Fe3O4
.(3)写出D与稀硫酸反应的化学方程式
Fe+H2SO4═FeSO4+H2↑
Fe+H2SO4═FeSO4+H2↑
.(4)物质A的一种用途
炼铁
炼铁
.分析:亚铁离子溶液属于浅绿色,根据D与硫酸反应生成浅绿色溶液F和气体E,所以D是金属铁,E是氢气,D物质在氧气中燃烧,也能生成B,可知铁在氧气中燃烧生成四氧化三铁,所以B是四氧化三铁,再根据A属于氧化物,且具有还原性,推出A物质,根据在化合物中正负化合价代数和为零,求出化合价,根据方程式的写法写出化学方程式.
解答:解:因为亚铁离子溶液属于浅绿色,D与硫酸反应生成浅绿色溶液F和气体E,所以F是亚铁离子溶液,金属与硫酸反应能生成盐和氢气,所以D属于铁就符合条件,铁与硫酸反应生成硫酸亚铁和氢气,E是氢气,铁在氧气中燃烧生成四氧化三铁,根据D物质在氧气中燃烧,也能生成B,可知B是四氧化三铁,A与四氧化三铁反应生成铁,说明A具有还原性,三大还原剂有:氢气、一氧化碳、碳,A属于氧化物,所以A是一氧化碳,一氧化碳与四氧化三铁反应生成铁和二氧化碳,所以C是二氧化碳;
(1)因为F是FeSO4,硫酸根化合价为-2价,根据化合物中正负化合价代数和为零,可知铁元素化合价是+2价;
(2)铁在氧气中燃烧生成四氧化三铁,从右往左读,数字是该元素右下角的数字,所以化学式为Fe3O4;
(3)D与稀硫酸反应的反应物是铁和硫酸,生成物是硫酸亚铁和氢气,氢气后面标上上升符号;
(4)一氧化碳具有可燃性,可以做燃料,具有还原性,能用来冶炼金属.
故答案为:(1)+2价;(2)Fe3O4;(3)Fe+H2SO4═FeSO4+H2↑;(4)炼铁.
(1)因为F是FeSO4,硫酸根化合价为-2价,根据化合物中正负化合价代数和为零,可知铁元素化合价是+2价;
(2)铁在氧气中燃烧生成四氧化三铁,从右往左读,数字是该元素右下角的数字,所以化学式为Fe3O4;
(3)D与稀硫酸反应的反应物是铁和硫酸,生成物是硫酸亚铁和氢气,氢气后面标上上升符号;
(4)一氧化碳具有可燃性,可以做燃料,具有还原性,能用来冶炼金属.
故答案为:(1)+2价;(2)Fe3O4;(3)Fe+H2SO4═FeSO4+H2↑;(4)炼铁.
点评:解答本题关键是找出突破口:D与硫酸反应生成浅绿色溶液F和气体E,推出D是铁,再根据铁燃烧的产物求出B的化学式,根据三大还原剂分析出A物质.

练习册系列答案
相关题目
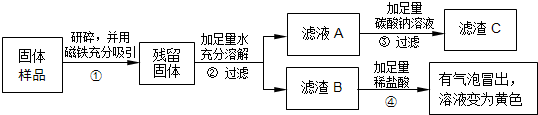
 (2013?盐城一模)红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如图所示.同学们对一包久置的“504双吸剂”固体样品很好奇,设计实验进行探究.
(2013?盐城一模)红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如图所示.同学们对一包久置的“504双吸剂”固体样品很好奇,设计实验进行探究.