题目内容
【题目】同学们用如图所示的操作展开了实验探究. 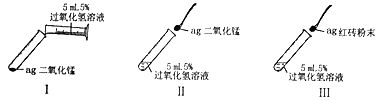
(1)【探究一】过氧化氢溶液与二氧化锰的加入顺序
实验Ⅰ向试管中缓缓加入过氧化氢溶液,反应的化学方程式是 .
实验Ⅱ中加入二氧化锰后,试管中快速产生大量气泡.实验Ⅰ、Ⅱ相比,可以得到平稳气流的是(填序号)
(2)【探究二】寻找新的催化剂
实验Ⅲ中加入红砖粉末后试管中产生大量气泡,检验该气体成分的方法是 , 这是利用了该气体具有的性质.待试管中不再产生气泡时,重新加入过氧化氢溶液,并再次检验气体,如此反复多次,观察现象,该实验目的是 . 将实验后的剩余物小心过滤,并将滤渣洗净、干燥、称量,所得固体仍为ag.通过上述过程得出的结论是 .
实验Ⅱ与实验Ⅲ对比,探究的问题是 .
实验拓展:查阅资料得知,CuO、CuSO4溶液、猪肝、马铃薯等都可以作过氧化氢分解的催化剂.下列有关催化剂的说法中正确的是 .
A.催化剂只能是固体
B.催化剂就是二氧化锰
C.催化剂也可能减慢化学反应速率
D.同一个化学反应可以有多种催化剂
E.使用催化剂能增加生成物的产量.
【答案】
(1)2H2O2 ![]() 2H2O+O2↑;Ⅰ
2H2O+O2↑;Ⅰ
(2)将带火星的木条伸入试管;助燃性;证明红砖粉末的化学性质没有改变;红砖粉可以做过氧化氢分解的催化剂;二氧化锰与红砖粉对过氧化氢分解的催化效果哪个更好;CD
【解析】解:【探究一】过氧化氢在二氧化锰催化下较快地分解,生成水和氧气;操作Ⅱ不能实现对药品用量及加入速度的控制,而操作Ⅰ通过缓缓加入溶液的方法控制药品的加入速度及用品,从而达到了控制反应速度的目的,所以两同学的实验现象不相同;因此,要得到平稳的氧气流应采取操作Ⅰ的方法进行制取.故填:2H2O2 ![]() 2H2O+O2↑;Ⅰ;
2H2O+O2↑;Ⅰ;
【探究二】检验氧气的方法是:将带火星的木条伸入试管中,若木条复燃,则证明产生的是氧气,氧气具有助燃性;待试管中不再产生气泡时,重新加入过氧化氢溶液,并再次检验气体,如此反复多次,观察现象,该实验目的是证明红砖粉末的化学性质没有改变.将实验后的剩余物小心过滤,并将滤渣洗净、干燥、称量,所得固体仍为ag.红砖粉加快了过氧化氢的反应速率,且其质量和化学性质没有改变,所以通过上述过程得出的结论是红砖粉可以做过氧化氢分解的催化剂;实验Ⅱ与实验Ⅲ对比,探究的是二氧化锰与红砖粉对过氧化氢分解的催化效果哪个更好;故填:将带火星的木条伸入试管;助燃性;红砖粉可以做过氧化氢分解的催化剂;二氧化锰与红砖粉对过氧化氢分解的催化效果哪个更好;
实验拓展:A.硫酸铜是一种液体,也可做该反应的催化剂,错误;
B.二氧化锰对其他化学反应不一定起到催化作用,错误;
C.催化剂不只是加快化学反应的速率,还能减慢化学反应的速率,正确;
D.根据题目的信息可知同一个化学反应可以有多种催化剂,正确;
E.催化剂只能改变化学反应的速率,并不能增加生成物的量,错误.
故选CD.
【考点精析】关于本题考查的催化剂的特点与催化作用,需要了解催化剂(触媒):在化学反应中能改变其他物质的化学反应速率,而本身的质量和化学性质在反应前后都没有发生变化的物质.(一变两不变)催化剂在化学反应中所起的作用叫催化作用才能得出正确答案.

【题目】某班学生在老师指导下探究铁与水蒸气的反应. 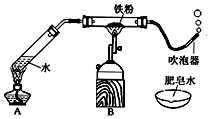
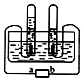
(1)按如图装好药品、连好装置(夹持仪器已略去).其中A装置的作用是 .
(2)加热一段时间后,灰色铁粉逐渐变黑,吹泡器连续吹出气泡,且气泡向上飞起;用燃着的木条靠近气泡,能产生爆鸣.该气体燃烧的化学方程式为 .
(3)同学们讨论后认为:铁与水蒸气反应生成的固体是“铁的一种氧化物”,玻璃管内的黑色固体中还可能含有“过量的铁”. 【查阅资料】铁有三种氧化物(FeO、Fe2O3、Fe3O4),其中FeO接触到空气会立即由黑色变为红棕色,铁的三种氧化物都不与硫酸铜溶液反应
【实验探究】
实验步骤 | 实验现象 | 实验结论 |
倒出玻璃管中黑色固体,平铺于白纸上 | 黑色固体不变色 | 黑色固体中一定没有(填物质名称) |
取上述黑色固体少许,装入试管,加入足量 | , 且有红色固体出现 | 黑色固体中一定含有 |
(4)【探究结论】铁与水蒸气发生置换反应,有关的化学方程式是
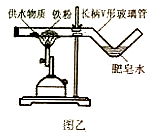
(5)【拓展创新】同学们利用微型仪器“长柄V形玻璃管”改进了图甲装置,设计出图乙装置,并分别选用湿棉花、湿粉笔、芦荟叶、芭蕉茎、氢氧化镁、氢氧化铜等作为供水剂,实验都获得成功 ①甲、乙装置相比,乙装置有很多优点,请你写一条:
②分析上述供水剂的供水原理,其中正确的是(填字母)
A.疏松、多孔的物质,有良好的吸水性和保水性能
B.新鲜的富水植物,在受热时水分容易释放出来
C.本身不含水的固体物质,不能用作供水剂.