题目内容
 (2010?南宁)如右图所示,当打开分液漏斗上的活塞让水滴入大试管中,可观察到以下现象:
(2010?南宁)如右图所示,当打开分液漏斗上的活塞让水滴入大试管中,可观察到以下现象:①U形管中a液面上升,b液面下降
②烧杯中的饱和溶液有晶体析出
则大试管中的固体M和烧杯中的饱和溶液N可能是( )
分析:U形管中a液面上升,b液面下降,说明试管中的压强减小,而烧杯中的饱和溶液有晶体析出,说明物质的溶解度发生了改变,可以据此解答.
解答:解:U形管中a液面上升,b液面下降,说明试管中的压强减小,而能够使压强减小的因素为试管中的温度降低,即该物质与水反应或溶于水的过程中吸收了热量,而烧杯中的饱和溶液有晶体析出,说明物质的溶解度随温度的降低而减小,分析题给的四个选项中:
A中氧化钙和水反应放热,使温度升高,压强增大,而B和C中的氢氧化钾和氢氧化钠溶于水要放出热量,故温度升高,压强增大,所以A、B、C,都不满足题意;
而D中的硝酸铵溶于水吸收热量,使温度降低,压强减小,从而使a中液面上升,而b中的液面下降,同时硝酸钾的溶解度随温度的降低而减小,满足题意.
故选D.
A中氧化钙和水反应放热,使温度升高,压强增大,而B和C中的氢氧化钾和氢氧化钠溶于水要放出热量,故温度升高,压强增大,所以A、B、C,都不满足题意;
而D中的硝酸铵溶于水吸收热量,使温度降低,压强减小,从而使a中液面上升,而b中的液面下降,同时硝酸钾的溶解度随温度的降低而减小,满足题意.
故选D.
点评:知道常见的物质溶于水时的吸热或者放热现象,并能够结合物理知识来解答问题.

练习册系列答案
 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案
相关题目
 (2010?南宁)如右图所示,光亮的铁钉在下列几种情况下,锈蚀速度由快到慢得顺序为( )
(2010?南宁)如右图所示,光亮的铁钉在下列几种情况下,锈蚀速度由快到慢得顺序为( )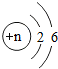 ,该原子核内有
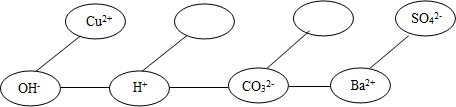
,该原子核内有 ”内,使其形成一个更为完整的复分解反应的知识网络.
”内,使其形成一个更为完整的复分解反应的知识网络.