题目内容
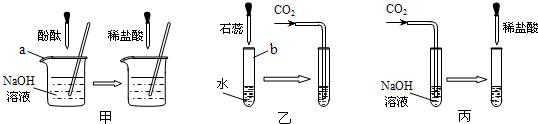
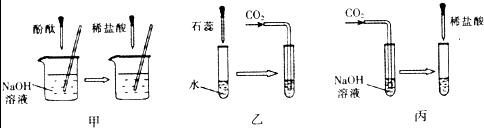
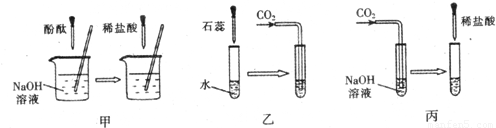
许多无明显现象的化学反应可通过滴加其它试剂的方法,使之产生明显的现象 以证明反应确实发生了.例如以下几个实验:
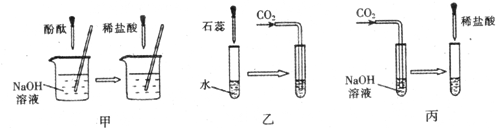
(1)实验甲中的NaOH与HCl恰好反应时,可观察到的现象是______;
实验乙中,可观察到的现象是______;化学方程式:______.
实验丙中,向NaOH溶液中通入一会儿CO2后,再滴入过量的稀HCl溶液,通入CO2后,滴入稀HCl溶液过程中溶液中溶质的种类在不断地变化中,其变化规律可能是______
A.2种-3种-2种-1种-2种 B.2种-3种-2种-1种
C.1种-2种-1种-2种 D.1种-3种-2种-1种-2种
(2)从研究原理得知,实验甲是通过检验反应前后溶液酸碱性的改变证明反应发生了,与之采用相同原理的还有实验______(填“乙”或“丙”);
(3)证明实验丙中NaOH与CO2发生了反应,除了可以滴加酸,还可滴加的试剂是______.
(4)若将含有盐酸的氯化钙溶液中和到中性,在不用指示剂的情况下,加入的试剂可以是______.
解:(1)氢氧化钠为碱性溶液,能使酚酞试液变红,当与盐酸恰好反应时,溶液呈中性,酚酞试液在中性溶液中显无色;二氧化碳与水可反应生成碳酸,碳酸可使石蕊变红,方程式是:CO2+H2O=H2CO3;
氢氧化钠溶液通入二氧化碳生成碳酸钠和水,碳酸钠可与盐酸反应生成氯化钠、水和二氧化碳,氢氧化钠和盐酸反应生成氯化钠和水,碳酸氢钠与盐酸反应生成氯化钠、水和二氧化碳;
若二氧化碳不足,则溶液中溶质是2种----氢氧化钠、碳酸钠,滴加稀盐酸,开始时盐酸不足,溶液中溶质是3种---氢氧化钠、碳酸钠、氯化钠,可能溶液中氢氧化钠的量较少,则随着盐酸的量的增加,可能溶液中氢氧化钠反应完毕,而碳酸钠未反应完,则溶质是2种---碳酸钠和氯化钠,恰好反应时溶质是1种---氯化钠,当滴加的盐酸过量时,溶质是2种---氯化钠、盐酸;
若通入的二氧化碳恰好与氢氧化钠溶液反应,则溶液中溶质是1种---碳酸钠,滴加稀盐酸不足时溶液中溶质是碳酸钠、氯化钠2种,恰好反应时溶质是氯化钠1种,盐酸过量时溶质是氯化钠、盐酸2种;
若通入的二氧化碳过量,则二氧化碳与碳酸钠和水反应又会生成碳酸氢钠,溶质可能是碳酸钠和碳酸氢钠2种(二氧化碳不能与碳酸钠完全反应),或二氧化碳恰好与生成的碳酸钠反应全部生成碳酸氢钠,滴加盐酸不足时溶质可能是3种(氯化钠、碳酸氢钠、碳酸钠),可能是2种(碳酸氢钠、氯化钠),恰好反应时溶质有1种---氯化钠,盐酸过量时溶质有2种---氯化钠、盐酸;
故可能是AC;
(2)实验甲是通过指示剂颜色的变化来判断反应的进行,与之原理相同的是乙;
(3)氢氧化钠与二氧化碳反应生成了碳酸钠,检验碳酸盐的存在可以使用加酸的方法,也可以使用加入可溶性钙或钡的化合物反应生成沉淀的方法;
(4)要除去氯化钙中的盐酸,在不用指示剂的情况下,加入的物质与盐酸反应时应该有明显的现象且不能生成新的杂质,因此可以使用加入碳酸钙的方法,过量的碳酸钙不溶于水,溶液依然是中性;
故答案为:(1)红色液体变为无色; 紫色液体变为红色; CO2+H2O=H2CO3; AC;
(2)乙;
(3)CaCl2;(合理均可);
(4)CaCO3.
分析:(1)酚酞试液在碱性溶液中为红色,在中性溶液中为无色;酸性溶液可使石蕊变红;二氧化碳与水可反应生成碳酸;依据二氧化碳和氢氧化钠反应原理,及氢氧化钠、碳酸钠与盐酸反应原理分析解答;
(2)实验甲是通过指示剂颜色的变化来判断反应的进行,与之原理相同的是乙;
(3)氢氧化钠与二氧化碳反应生成了碳酸钠,检验碳酸盐的存在可以使用加酸的方法,也可以使用加入可溶性钙或钡的化合物反应生成沉淀的方法;
(4)要除去氯化钙中的盐酸,可以使用加入碳酸钙的方法,且可使溶液变为中性.
点评:本题考查了常见的酸碱盐之间的反应,以及物质的检验和除杂的知识,完成此题,可以依据已有的知识进行,要求同学们在平时的学习中加强基础知识的储备,以便能够灵活应用,尤其对二氧化碳通入氢氧化钠溶液,滴加盐酸后溶液溶质的种类判断要仔细分析.
氢氧化钠溶液通入二氧化碳生成碳酸钠和水,碳酸钠可与盐酸反应生成氯化钠、水和二氧化碳,氢氧化钠和盐酸反应生成氯化钠和水,碳酸氢钠与盐酸反应生成氯化钠、水和二氧化碳;
若二氧化碳不足,则溶液中溶质是2种----氢氧化钠、碳酸钠,滴加稀盐酸,开始时盐酸不足,溶液中溶质是3种---氢氧化钠、碳酸钠、氯化钠,可能溶液中氢氧化钠的量较少,则随着盐酸的量的增加,可能溶液中氢氧化钠反应完毕,而碳酸钠未反应完,则溶质是2种---碳酸钠和氯化钠,恰好反应时溶质是1种---氯化钠,当滴加的盐酸过量时,溶质是2种---氯化钠、盐酸;
若通入的二氧化碳恰好与氢氧化钠溶液反应,则溶液中溶质是1种---碳酸钠,滴加稀盐酸不足时溶液中溶质是碳酸钠、氯化钠2种,恰好反应时溶质是氯化钠1种,盐酸过量时溶质是氯化钠、盐酸2种;
若通入的二氧化碳过量,则二氧化碳与碳酸钠和水反应又会生成碳酸氢钠,溶质可能是碳酸钠和碳酸氢钠2种(二氧化碳不能与碳酸钠完全反应),或二氧化碳恰好与生成的碳酸钠反应全部生成碳酸氢钠,滴加盐酸不足时溶质可能是3种(氯化钠、碳酸氢钠、碳酸钠),可能是2种(碳酸氢钠、氯化钠),恰好反应时溶质有1种---氯化钠,盐酸过量时溶质有2种---氯化钠、盐酸;
故可能是AC;
(2)实验甲是通过指示剂颜色的变化来判断反应的进行,与之原理相同的是乙;
(3)氢氧化钠与二氧化碳反应生成了碳酸钠,检验碳酸盐的存在可以使用加酸的方法,也可以使用加入可溶性钙或钡的化合物反应生成沉淀的方法;
(4)要除去氯化钙中的盐酸,在不用指示剂的情况下,加入的物质与盐酸反应时应该有明显的现象且不能生成新的杂质,因此可以使用加入碳酸钙的方法,过量的碳酸钙不溶于水,溶液依然是中性;
故答案为:(1)红色液体变为无色; 紫色液体变为红色; CO2+H2O=H2CO3; AC;
(2)乙;
(3)CaCl2;(合理均可);
(4)CaCO3.
分析:(1)酚酞试液在碱性溶液中为红色,在中性溶液中为无色;酸性溶液可使石蕊变红;二氧化碳与水可反应生成碳酸;依据二氧化碳和氢氧化钠反应原理,及氢氧化钠、碳酸钠与盐酸反应原理分析解答;
(2)实验甲是通过指示剂颜色的变化来判断反应的进行,与之原理相同的是乙;
(3)氢氧化钠与二氧化碳反应生成了碳酸钠,检验碳酸盐的存在可以使用加酸的方法,也可以使用加入可溶性钙或钡的化合物反应生成沉淀的方法;
(4)要除去氯化钙中的盐酸,可以使用加入碳酸钙的方法,且可使溶液变为中性.
点评:本题考查了常见的酸碱盐之间的反应,以及物质的检验和除杂的知识,完成此题,可以依据已有的知识进行,要求同学们在平时的学习中加强基础知识的储备,以便能够灵活应用,尤其对二氧化碳通入氢氧化钠溶液,滴加盐酸后溶液溶质的种类判断要仔细分析.

练习册系列答案
相关题目