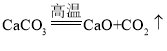题目内容
【题目】有一氧化碳和二氧化碳的混合气体40g,其中碳元素的质量分数为30%。使该混合气体通过足量的灼热氧化铜充分反应后。再将气体通入过量的石灰水中,能得到白色沉淀的质量为( )
A.30gB.50gC.100gD.150g
【答案】C
【解析】
整个过程中涉及到如下两个化学反应,据此结合碳元素质量守恒进行分析计算:
① ;②Ca(OH)2+CO2=CaCO3↓+H2O。
;②Ca(OH)2+CO2=CaCO3↓+H2O。
有一氧化碳和二氧化碳的混合气体40g,其中碳元素的质量分数为30%,则该混合气体中含有的碳元素的质量=40g×30%=12g,使该混合气体通过足量的灼热氧化铜充分反应后,由于一氧化碳能够与氧化铜在高温条件下反应生成二氧化碳,则充分反应后,得到的气体为纯净的二氧化碳,接下来将二氧化碳通入过量的石灰水中,二氧化碳能够与石灰水中的氢氧化钙反应生成白色的碳酸钙沉淀,根据质量守恒定律可得,整个过程中,碳元素质量守恒,则得到的碳酸钙中的碳元素的质量为12g,又因为碳酸钙中的碳元素的质量分数=![]() ,所以得到的碳酸钙的质量=12g÷12%=100g,即得到的白色沉淀的质量为100g,故选C。
,所以得到的碳酸钙的质量=12g÷12%=100g,即得到的白色沉淀的质量为100g,故选C。

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案
相关题目