题目内容
【题目】工业纯碱中常含有少量的氯化钠。某学习小组对其组成展开探究。现取24g纯碱样品,加入100g水使其完全溶解,再加入96g过量的氯化钙溶液.完全反应后,过滤洗涤、干燥得沉淀20g。完成下列问题:
(1)反应后溶液中含有的溶质是_____________(写 化学式);
(2)通过已知数据能求出的量有_____________( 写字母序号);
A反应后溶液的总质量
B参加反应的氯化钙的质量
C样品中碳酸钠的质量分数
D氯化钙溶液中溶质的质量分数
(3)计算纯碱样品中氯化钠的质量__________ (写出计算过程)。.
【答案】NaCl、CaCl2 ABC 2.8g
【解析】
(1)现取24g纯碱样品,加入100g水使其完全溶解,再加入96g过量的氯化钙溶液,氯化钙与碳酸钠反应生成碳酸钙沉淀和氯化钠,由于氯化钙过量,故反应后溶液中含有的溶质是:NaCl、CaCl2;
(2)A、反应后溶液的总质量为:24g+100g+96g-20g=200g,符合题意;
B、设参加反应的氯化钙的质量为x,样品中碳酸钠的质量为y
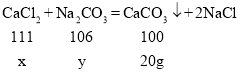
![]()
![]()
x=22.2g y=21.2g
参加反应的氯化钙的质量为22.2g,符合题意;
C、样品中碳酸钠的质量分数:
![]() ,符合题意;
,符合题意;
D、由于氯化钙过量,无法求出氯化钙溶液中溶质的质量,故无法求出氯化钙溶液中溶质的质量分数,不符合题意。
故选ABC。
(3)纯碱样品中氯化钠的质量为:24g-21.2g=2.8g。

 全能练考卷系列答案
全能练考卷系列答案 一课一练课时达标系列答案
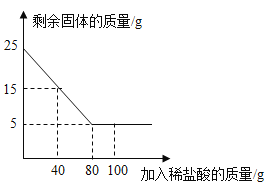
一课一练课时达标系列答案【题目】下列4个图像不能正确反映对应变化关系的是
|
|
|
|
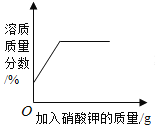
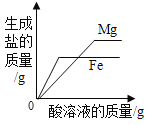
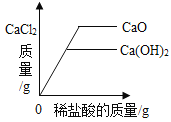
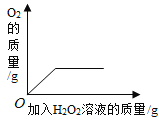
A20°C时,向一定量的硝酸钾不饱和溶液中加人硝酸钾固体 | B向等质量的镁粉和铁粉中分别逐滴加入同浓度的稀盐酸至过量 | C等质量CaO和Ca(OH)2中分别加入等浓度 的稀盐酸至过量 | D向 盛有少量二氧化锰的烧杯中不断地加入 过氧化氢溶液 |
A.AB.BC.CD.D