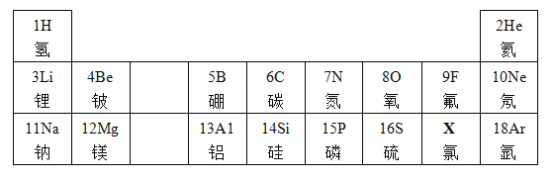
题目内容
【题目】某化学兴趣小组为了测定当地的石灰石(主要成分是CaCO3 )的质量分数,他们取25克样品放入烧杯中,向其中逐渐加入100克一定质量分数的稀盐酸(杂质不溶于水也不与酸反应),所用稀盐酸的质量与剩余固体的质量关系如图所示,请根据图中的数据进行计算:
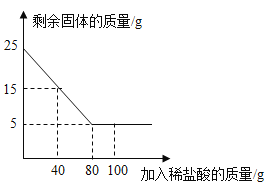
(1)当稀盐酸加到_____克时,样品与稀盐酸恰好完全反应。
(2)石灰石样品中CaCO3的质量分数为_____。(只填答案,不写计算过程)
(3)求恰好完全反应时所得溶液中溶质的质量分数。_____(要求计算步骤,精确到0.1%)
【答案】80 80% 24.3%
【解析】
(1)由图可知,当稀盐酸加到80克时,样品与稀盐酸恰好完全反应;
(2)石灰石样品中CaCO3的质量分数为:![]() ;
;
(3)解:设恰好完全反应时生成氯化钙的质量为x,生成二氧化碳的质量为y
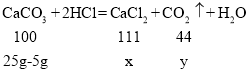
![]()
![]()
x=22.2g y=8.8g
恰好完全反应时所得溶液中溶质的质量分数为:
![]()
答:恰好完全反应时所得溶液中溶质的质量分数为24.3%。

 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案【题目】根据下列溶解度曲线和A物质的部分温度是的溶解度判断下列说法正确的是( )
温度/℃ | 0 | 20 | 40 | 60 | |
溶解度/g | A物质 | 20 | 28 | 45 | 60 |
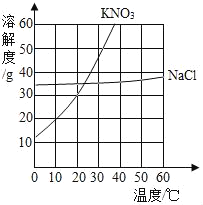
A. 由上图可知,KNO3和NaCl的溶解度均大于A 物质的溶解度
B. 10℃时,将40gNaCl放入50g水中,充分溶解,所得溶液是NaCl的不饱和溶液
C. 将30℃时NaCl、KNO3、和A物质的饱和溶液各降温至10℃,所得溶液的溶质质量分数大小为:KNO3>NaCl>A
D. 20℃时,将KNO3、NaCl和A物质各30g分别配制成恰好饱和溶液,所得溶液的质量大小为A>KNO3=NaCl
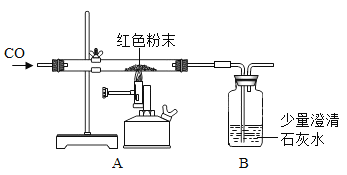
【题目】同学们对一包干燥的红色粉末氧化铁的含量进行测定。请你参与并回答有关问题。称取该粉末5.0g装入硬质玻璃管中,按下图在通风橱中进行实验。开始时缓缓通入CO气体,过一段时间后再加热使其充分反应。待反应完全后,停止加热,继续通CO气体至玻璃管冷却。反应前后称量相关装置和物质的总质量,其数据如下表(假定粉末中的杂质不参加反应,也不发生变化):
反应前 | 反应后 | |
①组 | 玻璃管和红色粉末的总质量为37.5g | 玻璃管和固体物质的总质量为36.3g |
②组 | 洗气瓶和所盛溶液的总质量为180.0g | 洗气瓶和瓶中物质的总质量为180.1g |
(交流讨论)
(1)开始实验时,在A装置中应_____(选序号“a.先通CO,排尽空气”“b.先加热红色粉末”)。
(2)选择①组的实验数据计算来确定红色粉末中氧化铁的质量分数是_____%,造成②组洗气瓶和瓶中物质的总质量增加量过小的原因是(写一点)_____。
(3)实验中观察到A装置反应管中的现象为_____。
(4)为了防止溶液倒吸,本实验停止加热前_____(填“需要”或“不需要”)先断开A和B的连接处。本实验中,为达到测定氧化铁含量的目的,可以用_____代替CO气体。
(反思评价)从环保角度看,该实验装置设计上不足之处是_____。