题目内容
通过化学实验可以认识物质的组成、性质与制取.
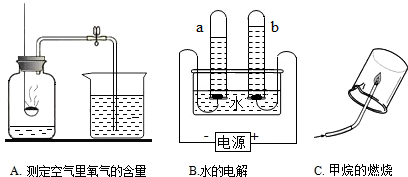
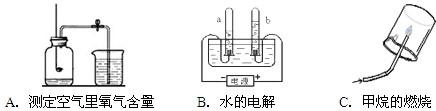
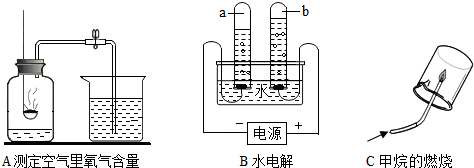
[探究1]研究常见物质组成.A、B、C都是教材上研究物质组成的实验.
(1)导致A实验测定结果偏小的可能原因有
(2)B实验的目的是
①确定水的组成 ②研究水的导电性 ③研究水分子的运动
(3)C实验通过验证反应产物并根据化学反应前后

[探究2]研究气体的制取、性质和收集
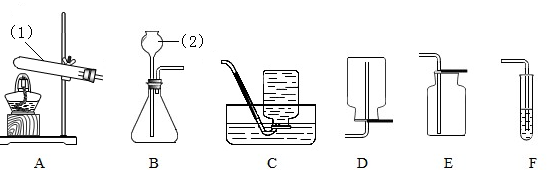
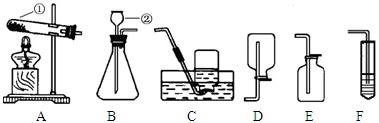
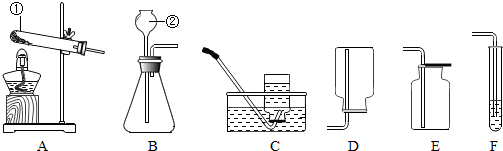
根据下列实验装置图,回答问题:

(1)写出标有序号的仪器名称:①
(2)小红将A与C相连,用高锰酸钾制取氧气,反应方程式为
实验操作有:a.停止加热 b.固定试管 c.将导管从水槽中取出 d.装药品和放棉花 e.加热,收集氧气.上述过程中缺少的一步操作是
(3)实验室制取二氧化碳气体,应选择的发生装置和收集装置分别选
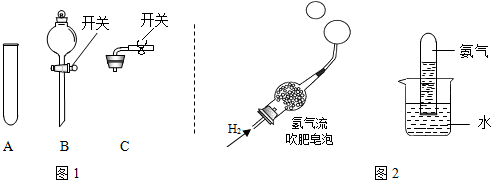
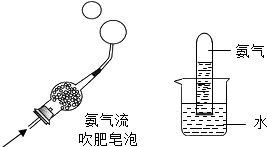
(4)化学兴趣小组的同学在研究氨气的性质时,做了如图1两个实验:
根据上述实验现象,写出氨气的两点性质
[探究1]研究常见物质组成.A、B、C都是教材上研究物质组成的实验.
(1)导致A实验测定结果偏小的可能原因有
红磷不足
红磷不足
(举一例).(2)B实验的目的是
①
①
(选择下列正确的序号填空)①确定水的组成 ②研究水的导电性 ③研究水分子的运动
(3)C实验通过验证反应产物并根据化学反应前后
元素
元素
种类不变来推断甲烷的组成.
[探究2]研究气体的制取、性质和收集
根据下列实验装置图,回答问题:

(1)写出标有序号的仪器名称:①
试管
试管
,②长颈漏斗
长颈漏斗
;(2)小红将A与C相连,用高锰酸钾制取氧气,反应方程式为
2KMnO4
K2MnO4+MnO2+O2↑
| ||
2KMnO4
K2MnO4+MnO2+O2↑
,
| ||
实验操作有:a.停止加热 b.固定试管 c.将导管从水槽中取出 d.装药品和放棉花 e.加热,收集氧气.上述过程中缺少的一步操作是
检查装置气密性
检查装置气密性
.(3)实验室制取二氧化碳气体,应选择的发生装置和收集装置分别选
BE
BE
.发生反应的化学方程式为CaCO3+2HCl=CaCl2+CO2↑+H2O
CaCO3+2HCl=CaCl2+CO2↑+H2O
.(4)化学兴趣小组的同学在研究氨气的性质时,做了如图1两个实验:
根据上述实验现象,写出氨气的两点性质
氨气密度比空气小
氨气密度比空气小
、氨气易溶于水
氨气易溶于水
.分析:[探究1](1)根据可能造成该结果的原因去分析;
(2)根据电解水的试验目的去分析;
(3)根据确定构成物质元素组成的方法去分析;
[探究2]
(1)根据常见仪器的名称分析即可;
(2)根据实验室用高锰酸钾制取氧气的反应原理及操作步骤分析即可;
(3)根据实验室制取二氧化碳的原理、发生装置及收集装置分析;
(4)根据图示所给的现象去分析原因.
(2)根据电解水的试验目的去分析;
(3)根据确定构成物质元素组成的方法去分析;
[探究2]
(1)根据常见仪器的名称分析即可;
(2)根据实验室用高锰酸钾制取氧气的反应原理及操作步骤分析即可;
(3)根据实验室制取二氧化碳的原理、发生装置及收集装置分析;
(4)根据图示所给的现象去分析原因.
解答:解:[探究1](1)若红磷不足以把集气瓶中的氧气消耗完,即集气瓶中仍有氧气剩余,这样将导致测定结果偏小.故答案为:红磷不足;
(2)电解水时得到氢气和氧气,根据元素守恒可确定水是由氢元素和氧元素组成的.故答案为:①;
(3)该实验可以观察到的现象有:烧杯壁上有水滴生产;迅速把烧杯倒转过来,向烧杯内注入少量澄清石灰水,澄清石灰水变浑浊.这两个现象说明该气体燃烧产物是水和二氧化碳,根据元素守恒可以确定该气体是由碳元素和氢元素构成的.故答案为:元素;
[探究2](1)根据常用仪器的名称可知①是试管,②是长颈漏斗,故答案为:试管;长颈漏斗;
(2)实验室由高锰酸钾制取氧气的方程式为:2KMnO4
K2MnO4+MnO2+O2↑,做有关气体的实验时一定首先检查装置的气密性,以防生成的气体外逸,根据题中给出的步骤可知该操作未检查装置的气密性,故答案为:检查装置的气密性;
(3)实验室用碳酸钙和盐酸制取二氧化碳,属于固液在常温下反应制取气体,所以发生装置选用B;二氧化碳能溶于水,且密度比空气大,因此可用向上排空气法收集,所以收集装置选用E;该反应的化学方程式为:CaCO3+2HCl=CaCl2+CO2↑+H2O,故答案为:BE;CaCO3+2HCl=CaCl2+CO2↑+H2O;
(4)第一个图观察到的现象是填充了该气体的气球上升,说明该气体密度比空气小;第二个图观察到的现象是水要上升,说明该气体易溶于水,故答案为:氨气密度比空气小;氨气易溶于水.
(2)电解水时得到氢气和氧气,根据元素守恒可确定水是由氢元素和氧元素组成的.故答案为:①;
(3)该实验可以观察到的现象有:烧杯壁上有水滴生产;迅速把烧杯倒转过来,向烧杯内注入少量澄清石灰水,澄清石灰水变浑浊.这两个现象说明该气体燃烧产物是水和二氧化碳,根据元素守恒可以确定该气体是由碳元素和氢元素构成的.故答案为:元素;
[探究2](1)根据常用仪器的名称可知①是试管,②是长颈漏斗,故答案为:试管;长颈漏斗;
(2)实验室由高锰酸钾制取氧气的方程式为:2KMnO4
| ||
(3)实验室用碳酸钙和盐酸制取二氧化碳,属于固液在常温下反应制取气体,所以发生装置选用B;二氧化碳能溶于水,且密度比空气大,因此可用向上排空气法收集,所以收集装置选用E;该反应的化学方程式为:CaCO3+2HCl=CaCl2+CO2↑+H2O,故答案为:BE;CaCO3+2HCl=CaCl2+CO2↑+H2O;
(4)第一个图观察到的现象是填充了该气体的气球上升,说明该气体密度比空气小;第二个图观察到的现象是水要上升,说明该气体易溶于水,故答案为:氨气密度比空气小;氨气易溶于水.
点评:此题属于综合性实验题,对同学们的要求比较高,这就要求同学们把握好课本上的基础知识.

练习册系列答案
相关题目
 通过化学实验可以认识物质的组成、性质与制取.
通过化学实验可以认识物质的组成、性质与制取.