题目内容
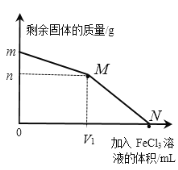
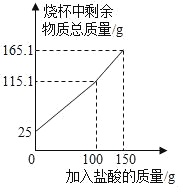
【题目】化学兴趣小组为了测定某贝壳中碳酸钙的含量,进行了如下实验:取洗净后的贝壳样品25g,捣碎后放入烧杯中,向烧杯中滴加稀盐酸(假设贝壳中其它物质不与稀盐酸反应,整个过程不考虑盐酸的挥发和气体的溶解。)实验测得烧杯中剩余物质的质量与加入盐酸的质量之间的关系如图所示。
(1)实验中将贝壳捣碎是为了_____。
(2)求贝壳中碳酸钙的质量分数。____
【答案】将贝壳捣碎的原因是增大了反应物的接触面积,促进反应的进行 90%
【解析】
(1)将贝壳捣碎的原因是增大了反应物的接触面积,促进反应的进行;
(2)解:根据质量守恒定律可得,生成的二氧化碳的质量为25g+100g﹣115.1g=9.9g,
设贝壳中碳酸钙的质量为x
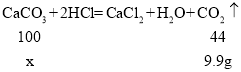
![]()
x=22.5
则贝壳中碳酸钙的质量分数为![]() ×100%=90%
×100%=90%
答:贝壳中碳酸钙的质量分数为90%。

练习册系列答案
相关题目
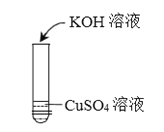
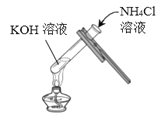
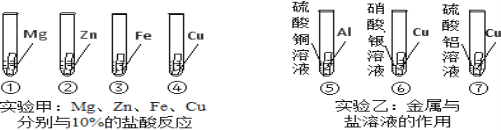
【题目】某兴趣小组在实验室中探究氢氧化钾的性质,请你参与他们的探究。
(实验过程与分析)
实验一 | 实验二 | 实验三 | |
实验操作 |
|
|
|
实验现象 | _______ | ______ | 无明显现象 |
实验结论 | 氢氧化钾能与硫酸铜发 生反应 | 氢氧化钾能与氯化铵发 生反应 | 氢氧化钾不能与硫酸 发生反应 |
(实验反思与拓展)
①某同学认为实验三的结论不正确。他改进了该实验方案,借助于酸碱指示剂,通过明显的现象证明氢氧化钾能与硫酸发生反应。简述他的实验方案:_____(写出操作方法和现象)。
②对于无明显现象的化学反应,可通过检验有新物质生成或检验_____的方法来证明物质间发生了化学反应。