题目内容
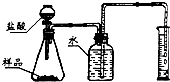 为了检验氢氧化钠是否已经全部变质,兴趣小组中小薇同学设计了如下实验方案:
为了检验氢氧化钠是否已经全部变质,兴趣小组中小薇同学设计了如下实验方案:准确称取一定质量的变质固体样品,放在图装置中,然后从分液漏斗中加入足量的盐酸,用排水法收集产生的二氧化碳,根据二氧化碳的体积和密度计算变质产物的质量,确定是否全部变质.
①你认为这个方案
②请你另外设计一个方案,并简要说明实验方法和结论.
考点:碱的化学性质,盐的化学性质
专题:常见的碱 碱的通性
分析:①称量的变质产物(含结晶水等)不是纯净的碳酸钠,再者二氧化碳会溶于水,造成的误差也比较大,故难以得出正确答案;
②要想验证氢氧化钠是否全部变质,可以在排除碳酸根离子的干扰的前提下来测定溶液的酸碱性.
②要想验证氢氧化钠是否全部变质,可以在排除碳酸根离子的干扰的前提下来测定溶液的酸碱性.
解答:解:①根据所给的实验方案,可以看出称量的是变质之后的产物,其中可能含有水分,再者把生成的二氧化碳通过水,会使部分二氧化碳溶于水,而造成较大的误差,从而得不出准确的答案,故这种方法不合适;
②要想验证氢氧化钠是否全部变质,由于碳酸钠显碱性,所以必须排除碳酸钠的干扰,然后再来测定溶液的酸碱性,如果在除去碳酸钠之后依然呈碱性,则说明氢氧化钡部分变质,否则就是全部变质.
故答案为:①不行;变质产物(含结晶水等)不是纯净的碳酸钠,同时CO2能溶于水不能用排水法集气,用排水法收集误差较大;
②将试样溶于水,加入足量CaCl2溶液后过滤,在滤液中滴加酚酞试液;如果滤液不变色,则氢氧化钠已经全部变质,如果滤液变红,则部分变质.
②要想验证氢氧化钠是否全部变质,由于碳酸钠显碱性,所以必须排除碳酸钠的干扰,然后再来测定溶液的酸碱性,如果在除去碳酸钠之后依然呈碱性,则说明氢氧化钡部分变质,否则就是全部变质.
故答案为:①不行;变质产物(含结晶水等)不是纯净的碳酸钠,同时CO2能溶于水不能用排水法集气,用排水法收集误差较大;
②将试样溶于水,加入足量CaCl2溶液后过滤,在滤液中滴加酚酞试液;如果滤液不变色,则氢氧化钠已经全部变质,如果滤液变红,则部分变质.
点评:熟练掌握氢氧化钠和碳酸钠的化学性质,并能选择合适的方法来检验氢氧化钠是否变质,即掌握可溶性碳酸盐的检验方法.

练习册系列答案
相关题目
下列各组离子在溶液中能大量共存的是( )
| A、Ca2+ Cl+ Na+ CO32- |
| B、H+ K+ NO3- OH- |
| C、H+ Na+ SO42- CO32- |
| D、K+ Na+ NO3- SO42- |
下列说法正确的是( )
| A、由同种元素组成的物质是单质 |
| B、纯净物一定是由同种分子构成 |
| C、最外层电子数是8的原子是稀有气体元素的原子 |
| D、质子数相同的粒子一定是同种元素 |
某气体单质的相对分子质量与氧气的相对分子质量之比为7:8,该气体是( )
| A、氮气 | B、氢气 |
| C、氖气 | D、一氧化碳 |
1985年科学家发现一种C60的物质,下列说法错误的是( )
| A、它的一个分子中含有60个碳原子 |
| B、它是一种新型化合物 |
| C、它是一种单质 |
| D、它由碳元素组成 |
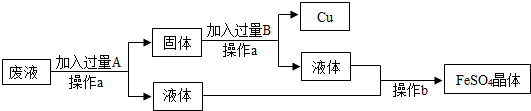
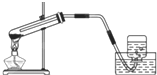 通过初中化学的学习,我们知道通过多种途径可获得氧气.
通过初中化学的学习,我们知道通过多种途径可获得氧气.