题目内容
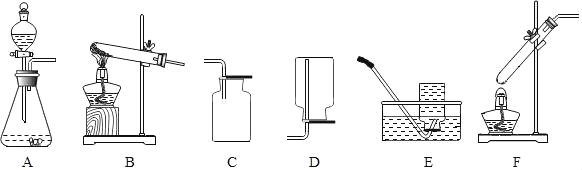
【题目】下列实验操作基本正确的是( )
A. 闻盐酸气味 B. 测溶液pH值
B. 测溶液pH值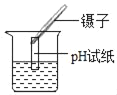
C. 稀释浓硫酸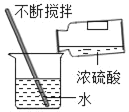 D. 加热液体
D. 加热液体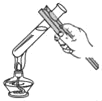
【答案】C
【解析】
A、闻气体的气味时,应用手在瓶口轻轻的扇动,使极少量的气体飘进鼻子中,不能将鼻子凑到集气瓶口去闻气体的气味,图中所示操作错误。
B、用pH试纸测定未知溶液的pH时,正确的操作方法为用玻璃棒蘸取少量待测液滴在干燥的pH试纸上,与标准比色卡对比来确定pH.不能将pH试纸伸入待测液中,以免污染待测液,图中所示操作错误。
C、稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,以使热量及时地扩散;一定不能把水注入浓硫酸中;图中所示操作正确。
D、给试管中的液体加热时,用酒精灯的外焰加热试管里的液体,且液体体积不能超过试管容积的1/3,图中液体超过试管容积的1/3、大拇指不能放在短柄上,图中所示操作错误。
故选:C。

 寒假学与练系列答案
寒假学与练系列答案【题目】某化学兴趣小组模拟“侯氏制碱法”制纯碱并进行后续实验。
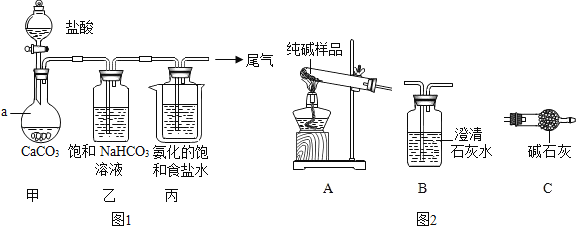
Ⅰ.制备纯碱:先以NaCl、NH3、CO2和水等为原料,用如图所示装置制取NaHCO3,得到的另一种产品NH4Cl,然后再将NaHCO3制成Na2CO3。
(1)写出仪器a的名称_____,装置丙中反应的化学方程式为_____。
(2)装置乙的作用是___________。为防止污染空气,尾气中的__________需要进行吸收处理。
(3)用装置丙中产生的NaHCO3制取Na2CO3时,需要进行的实验操作有___________、___________、___________。
Ⅱ.测定所得产品的组成
(4)检验纯碱样品中是否混有NaHCO3,请选择如图装置设计实验,并完成下表:
选择的装置(填编号) | 实验现象 | 实验结论 |
_____ | _____ | 样品中含NaHCO3 |
【题目】暖宝宝是一种防寒用品,暖宝宝的成分和发热的原理是什么?小明将如图的暖宝宝剪开内包装袋,倒出其中的粉末,发现粉末呈黑色。他在查阅资料后推测黑色粉末可能含有木炭粉、铁粉、氧化铜中的两种物质组成。

(猜想)黑色粉末是:猜想①铁粉和木炭粉;猜想②木炭粉和氧化铜;猜想③_____;
(查阅资料)(1)木炭与稀硫酸不反应,氧化铜与稀硫酸反应能产生蓝色溶液。
(2)暖宝宝中除了黑色粉末外,还含有氯化钠(俗名食盐)和水。
(进行实验)
实验操作步骤 | 实验现象 | 结论 |
①取少量黑色粉末于试管中,加足量稀硫酸 | 固体部分溶解,有气泡产生,溶液未变蓝色 | 黑色粉末中:一定含有_;一定不含__。 |
②取实验①的残渣灼烧,将内壁涂有澄清石灰水的小烧杯罩在上方 | ___ | 该黑色粉末中一定含有木炭粉。 |
(实验结论)猜想①正确。
(反思评价)(1)写出实验①的化学反应方程式:_____。
(2)宝宝贴在衣服上与空气接触后会发热的原因是_____。
(3)结合生活中常见现象,请你猜测暖宝宝中氯化钠的作用是_____。
【题目】在一支试管中放入一小段镁条(已擦去氧化膜),再向试管中加入一定量的盐酸,镁条表面有_____产生,反应的化学方程式是_____。
[发现问题]为了再次观察上述反应现象,小林同学用较长的镁条重做上述实验,但发现了异常现象,试管中出现了白色沉淀。
[实验验证1]小林同学针对两次实验的不同,设计对比实验方案,探究出现异常现象的原因。
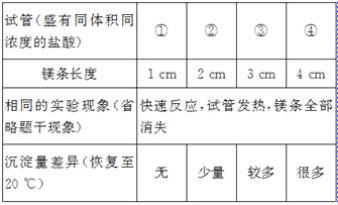
[得出结论]镁条与盐酸反应产生白色沉淀与_____有关。
[追问]白色沉淀是什么物质?
[查阅资料]①20 ℃时,100 g水中最多能溶解氯化镁54.8 g;
②镁能与热水反应产生一种碱和氢气;
③氯化银既不溶于水也不溶于稀硝酸。
[做出猜想]猜想一:镁;猜想二:氯化镁;猜想三:氢氧化镁,猜想的依据是_____(用化学方程式表示)。
[实验验证2]将白色沉淀洗涤干净,分别取少量沉淀于A、B、C试管中,进行如表实验:
试管 | 操作 | 现象 | 结论 |
A | 加入足量盐酸 | _____,白色沉淀_____ | 猜想一不正确,但这种白色沉淀能溶于盐酸 |
B | 加入足量水 | 白色沉淀_____ | 猜想二不正确 |
C | 加入适量稀硝酸 | 白色沉淀消失 | 原白色沉淀中含有的离子是:Mg2+、_____ |
继续滴加几滴硝酸银溶液 | 出现大量白色沉淀 |