题目内容
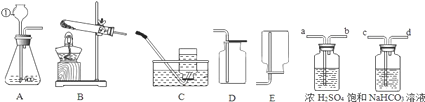
【题目】某校化学探究小组为研究氢氧化钠、氢氧化钙两种溶液的化学性质,进行如下实验。
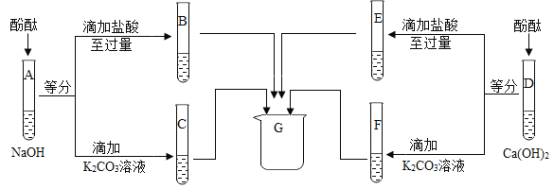
(1)A、D中酚酞均变______色,说明两种溶液都呈碱性。
(2)E中溶液中含有的溶质有______(指示剂除外)。
(3)请描述②中的实验现象______。
(4)将四支试管内的物质倒入G中混合后得到白色沉淀和无色溶液。则G中一定含有的溶质是______,可能含有的溶质是______。
【答案】红 氯化钙、氯化氢 产生白色沉淀,溶液仍然是红色 氯化钠、氯化钾 氯化钙
【解析】
(1)A、D中酚酞均变红色,说明两种溶液都呈碱性。
故填:红。
(2)E中溶液中含有的溶质有反应生成的氯化钙和过量的氯化氢。
故填:氯化钙、氯化氢。
(3)②中氢氧化钙和碳酸钾反应生成碳酸钙沉淀和氢氧化钾,观察到产生白色沉淀,溶液仍然是红色。
故填:产生白色沉淀,溶液仍然是红色。
(4)将四支试管内的物质倒入G中混合后得到白色沉淀(碳酸钙),说明盐酸完全反应,得到无色溶液,说明溶液不显碱性,则G中一定含有的溶质是反应生成的氯化钠和氯化钾,可能含有的溶质是氯化钙。
故填:氯化钠、氯化钾;氯化钙。

 名校课堂系列答案
名校课堂系列答案【题目】请参与下列实验探究:
(实验探究)
实验内容 | 记录数据 |
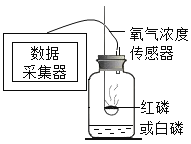
A.借助新型传感设备探究红磷、白磷在空气中燃烧时的耗氧情况
| 燃烧红磷:瓶内剩余氧气的体积分数为8.85% 燃烧白磷:瓶内剩余氧气的体积分数为3.21% |
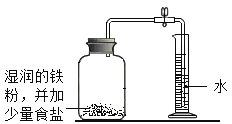
B.用铁生锈原理测定空气中氧气的体积分数
| 反应前测定:广囗瓶容积(扣除药品、导管和瓶塞所占容积)为125.0mL 反应后测定:进入广口瓶中水的体积 为25.0mL |
(1)红磷和白磷是由相同的磷元素组成的不同___(填“化合物”或“单质”)。进行A实验时,燃烧反应的化学方程式可表示为___。
(2)实验A的测定结果是在操作无误、装置不漏气,红磷、白磷均足量的情况下得到的,请从燃烧条件的角度说明红磷、白磷耗氧差异较大的主要原因___。
(3)实验B中,下列属于为加快实验进程而采取的措施是___和___(填数字编号)。
①在集气瓶中进行 ②塞紧瓶塞不漏气③使用铁粉而不使用铁丝④加少量食盐
(4)铁生锈的实质是铁与___(写化学式)发生了化学反应。根据表中记录数据,可计算出空气中氧气的体积分数为___。
(反思与拓展)铜在潮湿的空气中生成铜绿(化学式为Cu2(OH)2CO3)时也能耗氧,从化学式可以看出,铜绿的生成是铜与水及空气中的___发生反应的过程,所以,实验B___(填“能”或“不能”)用铜粉代替铁粉。
【题目】某化学兴趣小组用实验室常用药品(或溶液)对“NaOH溶液与稀盐酸是否恰好完全反应”进行探究。
(知识卡片):氯化钠溶液显中性。氯化铜易溶于水。
(实验探究):
(1)方案Ⅰ:某同学先向试管中加入约2mLNaOH溶液,再滴入几滴酚酞溶液,溶液变红。然后慢慢滴入稀盐酸,边滴边振荡,直至溶液恰好变为无色。
①实验结论_________。
②从微观的角度分析,该反应的实质是_________。
③在滴入稀盐酸的过程中,若观察到有少量气泡出现,请分析产生气泡的可能原因_______(用化学方程式表示)。
(2)方案Ⅱ:
实验步骤 | 实验现象 | 结论 |
取2mLNaOH溶液于试管中,滴入一定量的稀盐酸,振荡后加入镁条 | 若_______ | 稀盐酸过量 |
若没有明显现象 | NaOH溶液与稀盐酸恰好完全反应 |
(实验反思):
(3)另有同学提出方案Ⅱ不能证明NaOH溶液与稀盐酸恰好完全反应,其原因是______。
(4)除以上方案外,下列哪些物质单独使用,也能证明“NaOH 溶液与稀盐酸是否恰好完全反应”_________ (填序号)。
A 铜片 B pH试纸 C 氧化铜 D 紫色石蕊试液