题目内容
【题目】符合事实且化学方程式书写正确的是( )
A.用硝酸银溶液鉴别稀盐酸和稀硫酸:AgNO3+HCl═AgCl↓+HNO3
B.铁与盐酸反应制取氢气:2Fe+6HCl═2FeCl3+3H2↑
C.正常雨水 pH 值约为 5.6 的原因:CO2+H2O═H2CO3
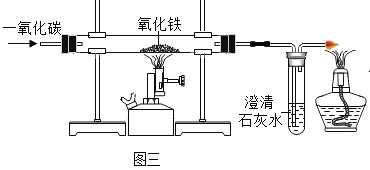
D.点燃法除去 CO2 中混有少量的 CO:2CO+O2![]() 2CO2
2CO2
【答案】C
【解析】
A、不能用硝酸银鉴别稀盐酸和稀硫酸,是因为硝酸银和盐酸反应生成白色沉淀氯化银,和稀硫酸反应生成硫酸银,硫酸银微溶于水,生成的量多了会形成白色沉淀,故选项错误;
B、铁和稀盐酸反应生成氯化亚铁和氢气,故选项错误;
C、正常雨水 pH 值约为 5.6 的原因是二氧化碳能和水反应生成碳酸,反应的化学方程式:CO2+H2O═H2CO3,故选项正确;
D、二氧化碳中的一氧化碳不能被点燃,故选项错误。
故选:C。

【题目】实验室有一瓶标签模糊的氢氧化钠溶液,为了测定其溶质质量分数,小明进行了如下实验:①取一洁净的锥形瓶称量,然后往其中加入一定量的氢氧化钠溶液,并滴入几滴酚酞试液(质量忽略不计),重新称量;②往上述锥形瓶中加入溶质质量分数为7.3%的盐酸,边加边振荡,溶液红色褪去时,再次称量。数据如下表:回答下列问题:
锥形瓶/g | 锥形瓶+氢氧化钠溶液/g | 锥形瓶+反应后溶液/g | |
质量/g | 35.5 | 60.5 | 110.5 |
(1)根据表中数据,通过计算确定该瓶氢氧化钠溶液的溶质质量分数_________。
(2)小建用pH试纸测得小明实验反应后锥形瓶内溶液的pH为4,则小明测出氢氧化钠溶液的质量分数比实际浓度_________(选填“偏大”或“偏小”),造成这一偏差的原因是________。
【题目】K2CO3和KNO3在不同温度时的溶解度如下。
温度/℃ | 20 | 30 | 50 | 60 | 80 | |
溶解度(g/100g 水) | K2CO3 | 110 | 114 | 121 | 126 | 139 |
KNO3 | 31.6 | 45.8 | 85.5 | 110 | 169 | |
某KNO3样品中含有少量K2CO3,其提纯过程如下:
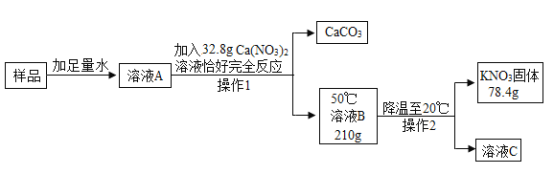
①提纯过程中涉及的化学反应方程式是_____。
②溶液 A 中加 Ca(NO3)2溶液恰好完全反应的目的是_____。下列试剂中可以替代Ca(NO3)2 溶液的是_____(填字母)。
a CaCl2 b Ba(NO3)2 c Ca(OH)2 d BaCl2
③溶液A、B、C 中,一定属于饱和溶液的是_____(填字母)。
④样品中钾元素的质量为_____g(精确到0.1)。
⑤若要测定样品中KNO3 的纯度,还需测定的量是_____。