题目内容
某化学兴趣小组的同学采用了如图所示装置测定空气中氧气含量.【实验步骤】:在由两个注射器组成的密闭系统中留有25mL空气,给装有细铜丝的玻璃管加热,同时缓慢推动两个注射器活塞,至玻璃管内的铜丝在较长时间内无进一步变化时停止加热,待冷却至室温,将气体全部推至一个注射器内,观察密闭系统内空气体积变化.
【实验分析】:(1)在实验加热过程中,交替缓慢推动两个注射器活塞的目的是______.
(2)写出该实验过程中玻璃管内的现象为______
写出该反应的文字表达式______

【答案】分析:本题是测定空气中氧气的含量,我们常用燃烧红磷或白磷的方法,因为磷燃烧生成白色固体五氧化二磷,几乎不占空间,使得内外产生气压差,从而得到正确的结论.本题用的是铜丝,生成物是氧化铜固体,现象是红色变黑色.因此在选择可燃物时,必须考虑到:燃烧的条件;生成物的状态;不与空气中其他物质发生反应.实验反思中,实验误差较大的原因有:①装置气密性不好;②铜丝的量不足,氧气没有完全消耗等.
解答:解:(1)交替缓慢推动两个注射器活塞的目的是让氧气充分反应,故答案为:使空气中的氧气与铜丝充分反应
(2)现象是红色变黑色,铜和氧气在加热的条件下生成氧化铜.故答案为:红色变黑色;铜+氧气 氧化铜
氧化铜
(3)小强实验操作均正确时,剩余气体是20mL,实验得出的结论为:氧气约占空气体积的五分之一.实验误差较大的原因有:①装置气密性不好;②铜丝的量不足,氧气没有完全消耗等.故答案为:20mL;氧气约占空气体积的五分之一;装置不严密.
点评:本考点考查的是空气中氧气含量的探究实验,根据实验操作图,回忆实验中现象,由实验中的注意事项,对实验结果进行评价,从而理解该实验的探究目的.对实验结果进行评价,是近几年中考的重点之一,要好好把握.本考点主要出现在实验题中.
解答:解:(1)交替缓慢推动两个注射器活塞的目的是让氧气充分反应,故答案为:使空气中的氧气与铜丝充分反应
(2)现象是红色变黑色,铜和氧气在加热的条件下生成氧化铜.故答案为:红色变黑色;铜+氧气
 氧化铜
氧化铜(3)小强实验操作均正确时,剩余气体是20mL,实验得出的结论为:氧气约占空气体积的五分之一.实验误差较大的原因有:①装置气密性不好;②铜丝的量不足,氧气没有完全消耗等.故答案为:20mL;氧气约占空气体积的五分之一;装置不严密.
点评:本考点考查的是空气中氧气含量的探究实验,根据实验操作图,回忆实验中现象,由实验中的注意事项,对实验结果进行评价,从而理解该实验的探究目的.对实验结果进行评价,是近几年中考的重点之一,要好好把握.本考点主要出现在实验题中.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
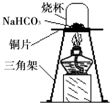 12、碳酸氢钠(NaHCO3)俗称小苏打,常用于食品和医药工业.某化学兴趣小组的同学对碳酸氢钠的性质进行探究.
12、碳酸氢钠(NaHCO3)俗称小苏打,常用于食品和医药工业.某化学兴趣小组的同学对碳酸氢钠的性质进行探究.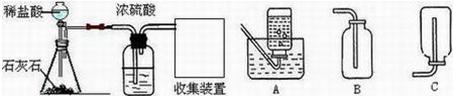
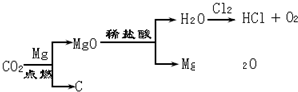
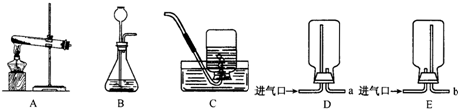
 (2012?烟台)某化学兴趣小组的同学用如图所示装置进行实验(装置气密性良好),先关闭止水夹,将足量的氢氧化钠溶液滴入烧瓶中,充分吸收掉二氧化碳后,再打开止水夹.
(2012?烟台)某化学兴趣小组的同学用如图所示装置进行实验(装置气密性良好),先关闭止水夹,将足量的氢氧化钠溶液滴入烧瓶中,充分吸收掉二氧化碳后,再打开止水夹. 某化学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液,并用其测定某稀盐酸中溶质的质量分数.
某化学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液,并用其测定某稀盐酸中溶质的质量分数.