题目内容
【题目】取MgCl2和NaCl的固体混合物10g做如下实验.请根据图中实验及数据进行计算.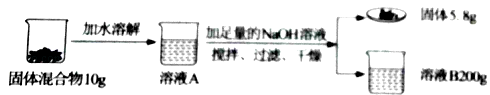

(1)MgCl2中镁元素和氯元素的质量比为
(2)计算溶液B中NaCl的质量分数(写出计算过程).
(3)要配制与溶液B相同质量分数的NaCl溶液200g,需要质量分数为24.4%的NaCl溶液的质量是多少?(写出计算过程)
【答案】
(1)24:71
(2)
解:MgCl2中镁元素和氯元素的质量比为为24:(35.5×2)=24:71
设混合物中氯化镁的质量为x,生成的氯化钠的质量为y
MgCl2+2NaOH= | Mg(OH)2↓+ | 2NaCl |
95 | 58 | 117 |
x | 5.8g | y |
![]() =
= ![]() =
= ![]()
x=9.5g
y=11.7g
溶液B中NaCl的质量分数为 ![]() ×100%=7.95%
×100%=7.95%
(3)
解:设质量分数为24.4%的NaCl溶液的质量为z
由于稀释过程中溶质的质量不变
24.4%z=200g×7.95%
z≈65.2g
【解析】解:
MgCl2中镁元素和氯元素的质量比为为24:(35.5×2)=24:71
设混合物中氯化镁的质量为x,生成的氯化钠的质量为y
MgCl2+2NaOH= | Mg(OH)2↓+ | 2NaCl |
95 | 58 | 117 |
x | 5.8g | y |
![]() =
= ![]() =
= ![]()
x=9.5g
y=11.7g
溶液B中NaCl的质量分数为 ![]() ×100%=7.95%
×100%=7.95%
设质量分数为24.4%的NaCl溶液的质量为z
由于稀释过程中溶质的质量不变
24.4%z=200g×7.95%
z≈65.2g
答:(1)MgCl2中镁元素和氯元素的质量比为 24:71.(2)溶液B中NaCl的质量分数为7.95%.(3)要配制与溶液B相同质量分数的NaCl溶液200g,需要质量分数为24.4%的NaCl溶液的质量是65.2g.
【考点精析】通过灵活运用根据化学反应方程式的计算,掌握各物质间质量比=系数×相对分子质量之比即可以解答此题.

 阅读快车系列答案
阅读快车系列答案