题目内容
氧气是空气中的重要成分,能够提供呼吸支持燃烧,下列方法能够用于实验室可以用来制备氧气且产物有盐、氧化物和单质三种的是( )A.高锰酸钾加热
B.氯酸钾(二氧化锰)共热
C.双氧水催化分解
D.电解水
【答案】分析:盐是由金属离子(或铵根离子)和酸根离子组成的化合物;氧化物是指有两种元素组成且一种是氧元素的化合物;由同种元素组成的纯净物是单质;据此进行分析判断.
解答:解:A、高锰酸钾能够用于实验室可以用来制备氧气,高锰酸钾在加热条件下生成锰酸钾、二氧化锰和氧气,锰酸钾是由钾离子和高锰酸根离子构成的,属于盐;二氧化锰是由两种元素组成且有一种是氧元素,属于氧化物;氧气是由一种元素组成的纯净物,属于单质;故选项符合题意.
B、氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,生成物只有两种,故选项不符合题意.
C、双氧水在二氧化锰的催化作用下生成水和氧气,生成物只有两种,故选项不符合题意.
D、电解水生成氢气和氧气,不能用于实验室可以用来制备氧气;且生成物只有两种,故选项不符合题意.
故选A.
点评:本题难度不大,掌握实验室制取氧气的反应原理及盐、氧化物和单质的特征是正确解答本题的关键.
解答:解:A、高锰酸钾能够用于实验室可以用来制备氧气,高锰酸钾在加热条件下生成锰酸钾、二氧化锰和氧气,锰酸钾是由钾离子和高锰酸根离子构成的,属于盐;二氧化锰是由两种元素组成且有一种是氧元素,属于氧化物;氧气是由一种元素组成的纯净物,属于单质;故选项符合题意.
B、氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,生成物只有两种,故选项不符合题意.
C、双氧水在二氧化锰的催化作用下生成水和氧气,生成物只有两种,故选项不符合题意.
D、电解水生成氢气和氧气,不能用于实验室可以用来制备氧气;且生成物只有两种,故选项不符合题意.
故选A.
点评:本题难度不大,掌握实验室制取氧气的反应原理及盐、氧化物和单质的特征是正确解答本题的关键.

练习册系列答案
相关题目
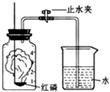
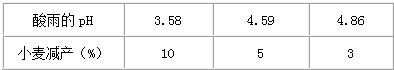
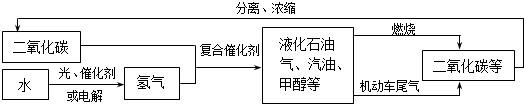
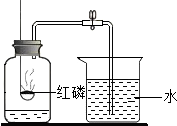 空气是一种重要的自然资源.通过半年的初中化学学习,我们可以从化学的视角来进一步认识空气.
空气是一种重要的自然资源.通过半年的初中化学学习,我们可以从化学的视角来进一步认识空气. 认识燃烧,科学地利用燃烧,使燃烧为人类服务是十分重要的.为验证可燃物燃烧的条件,某兴趣小组进行了如下探究活动.
认识燃烧,科学地利用燃烧,使燃烧为人类服务是十分重要的.为验证可燃物燃烧的条件,某兴趣小组进行了如下探究活动.