题目内容
质量分数为10%的盐酸,要使溶质的质量分数增大,可采用的方法是( )
【答案】分析:溶质的质量分数= ×100%,所以要使溶质的质量分数增大,可增加溶质的质量或减少溶剂的质量.
×100%,所以要使溶质的质量分数增大,可增加溶质的质量或减少溶剂的质量.
解答:解:A、盐酸溶液的溶质是氯化氢气体,氯化氢气体极易溶于水,所以向10%的盐酸中通氯化氢气体,就会增加溶质的质量,增大溶质的质量分数.故A正确;
B、理论上加热蒸发溶剂,溶剂质量减少,可增大溶质的质量分数,但盐酸溶液在加热的时候会挥发出氯化氢气体,即溶质质量也会减少,所以加热蒸发盐酸溶液溶质的质量分数不一定会增大.故B错误;
C、稀盐酸和浓盐酸混合后,溶质的质量分数会比原来稀盐酸的质量分数大,所以质量分数为10%的盐酸中加入38%的浓盐酸,溶质的质量分数会增大.故C正确;
D、加水相当于溶液的稀释,溶液中溶剂的质量增大,所以溶质的质量分数减小.故D错误.
故选AC.
点评:此题考查的是溶质质量分数的有关知识,溶质质量分数的增减的判断,关键是掌握溶质质量分数的公式.此题考查的知识点单一,较为简单.
 ×100%,所以要使溶质的质量分数增大,可增加溶质的质量或减少溶剂的质量.
×100%,所以要使溶质的质量分数增大,可增加溶质的质量或减少溶剂的质量.解答:解:A、盐酸溶液的溶质是氯化氢气体,氯化氢气体极易溶于水,所以向10%的盐酸中通氯化氢气体,就会增加溶质的质量,增大溶质的质量分数.故A正确;
B、理论上加热蒸发溶剂,溶剂质量减少,可增大溶质的质量分数,但盐酸溶液在加热的时候会挥发出氯化氢气体,即溶质质量也会减少,所以加热蒸发盐酸溶液溶质的质量分数不一定会增大.故B错误;
C、稀盐酸和浓盐酸混合后,溶质的质量分数会比原来稀盐酸的质量分数大,所以质量分数为10%的盐酸中加入38%的浓盐酸,溶质的质量分数会增大.故C正确;
D、加水相当于溶液的稀释,溶液中溶剂的质量增大,所以溶质的质量分数减小.故D错误.
故选AC.
点评:此题考查的是溶质质量分数的有关知识,溶质质量分数的增减的判断,关键是掌握溶质质量分数的公式.此题考查的知识点单一,较为简单.

练习册系列答案
相关题目
浩瀚的海洋中蕴藏着丰富的自然资源,现摘取部分海水综合利用的方案如下:
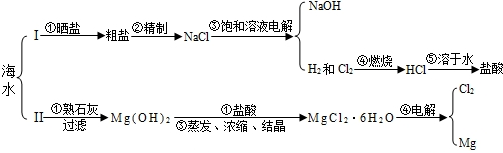
请根据下列部分酸碱盐溶解性表回答下列问题:
(1)除去粗盐中混有的少量不溶性杂质,下列操作顺序正确的是 (填编号,下同)
①过滤 ②溶解 ③蒸发
(2)过滤后所得滤液仍然浑浊,可能的原因是 ;
①滤纸破损 ②过滤时漏斗里的液面高于滤纸的边缘 ③漏斗颈下端管口没有紧靠烧杯内壁.
(3)如果海水中含有的可溶性杂质主要为CaCl2、MgSO4,则方案Ⅰ中步骤②“精制”时:欲沉淀杂质CaCl2,一般加入稍过量的碳酸钠溶液,此反应方程式为 ;
如果井水或溪水中含有Ca2+、Mg2+,这种水称作 ,如果在这种水中加入肥皂,会出现 .
(4)方案Ⅱ中步骤①生成Mg(OH)2的反应方程式为 ;
如果熟石灰是用海边的贝壳(主要成分为CaCO3)生成的,则生产熟石灰的反应方程式为: 、 .
(5)方案Ⅱ中除步骤①中用过滤外,还要用到“过滤”步骤的是 (填序号).
(6)下图是某种加钙食盐包装袋标签上的部分说明文字(Ca-40,C-12,O-16):
如果每袋加钙食盐含Ca为0.5%,则含CaCO3的质量为 g.
(7)某化工厂为测定氯化钠样品的纯度,取30g氯化钠样品(杂质为氯化钙)溶于水制成252g溶液,再加入53g溶质质量分数为10%的碳酸钠溶液,恰好完全反应.求:
①样品中杂质CaCl2的质量;
②样品中氯化钠的质量;
③样品中氯化钠的质量分数;
④反应后所得溶液中溶质的质量分数.

请根据下列部分酸碱盐溶解性表回答下列问题:
| OH- | Cl- | SO42- | CO32- | |
| Na+ | 溶 | 溶 | 溶 | 溶 |
| Ca2+ | 微 | 溶 | 微 | 不 |
| Ba2+ | 溶 | 溶 | 不 | 不 |
| Mg2+ | 不 | 溶 | 溶 | 不 |
①过滤 ②溶解 ③蒸发
(2)过滤后所得滤液仍然浑浊,可能的原因是
①滤纸破损 ②过滤时漏斗里的液面高于滤纸的边缘 ③漏斗颈下端管口没有紧靠烧杯内壁.
(3)如果海水中含有的可溶性杂质主要为CaCl2、MgSO4,则方案Ⅰ中步骤②“精制”时:欲沉淀杂质CaCl2,一般加入稍过量的碳酸钠溶液,此反应方程式为
如果井水或溪水中含有Ca2+、Mg2+,这种水称作
(4)方案Ⅱ中步骤①生成Mg(OH)2的反应方程式为
如果熟石灰是用海边的贝壳(主要成分为CaCO3)生成的,则生产熟石灰的反应方程式为:
(5)方案Ⅱ中除步骤①中用过滤外,还要用到“过滤”步骤的是
(6)下图是某种加钙食盐包装袋标签上的部分说明文字(Ca-40,C-12,O-16):
| 配料表:氯化钠、食用碳酸钙、碘酸钾 净含量:500g 成分表:氯化钠≥88% 钙(以Ca计)(0.5-1.3)% 碘(以I计)(20-50)mg/kg |
(7)某化工厂为测定氯化钠样品的纯度,取30g氯化钠样品(杂质为氯化钙)溶于水制成252g溶液,再加入53g溶质质量分数为10%的碳酸钠溶液,恰好完全反应.求:
①样品中杂质CaCl2的质量;
②样品中氯化钠的质量;
③样品中氯化钠的质量分数;
④反应后所得溶液中溶质的质量分数.
 (2011?南京)某化学兴趣小组进行溶液的配置和粗盐的初步提纯实验.
(2011?南京)某化学兴趣小组进行溶液的配置和粗盐的初步提纯实验.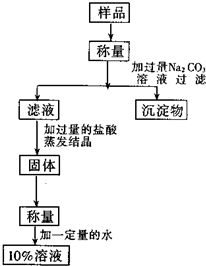 用含有少量氯化钙的氯化钠固体配置溶质的质量分数为10%的氯化钠溶液,设计如图所示操作方案.请回答:
用含有少量氯化钙的氯化钠固体配置溶质的质量分数为10%的氯化钠溶液,设计如图所示操作方案.请回答: (2013?长宁区一模)某化学兴趣小组欲进行粗盐的初步提纯和溶液的配制实验.
(2013?长宁区一模)某化学兴趣小组欲进行粗盐的初步提纯和溶液的配制实验.