题目内容
实验室欲配制50g质量分数为10%的氯化钠溶液.
(1)配制步骤及过程可以概括为以下四步:
①
②
③
④
(2)为了加快氯化钠的溶解,通常采用
(3)若使用的是含有泥沙的粗盐,应先进行提纯,其操作步骤为
(4)实验中,若NaCl末经干燥就直接配制溶液,则溶质的质量分数将
(5)量取水的体积,读数时,若俯视刻度线,则溶液的质量分数将
(1)配制步骤及过程可以概括为以下四步:
①
计算
计算
;②
称量
称量
;③
量取
量取
;④
溶解
溶解
.(2)为了加快氯化钠的溶解,通常采用
用玻璃棒不断搅拌
用玻璃棒不断搅拌
、加热
加热
、将食盐颗粒粉碎
将食盐颗粒粉碎
等措施.(3)若使用的是含有泥沙的粗盐,应先进行提纯,其操作步骤为
溶解
溶解
、过滤
过滤
、蒸发
蒸发
、然后烘干,以备使用.(4)实验中,若NaCl末经干燥就直接配制溶液,则溶质的质量分数将
偏低
偏低
(填“偏低”、“偏高”或“不变”).(5)量取水的体积,读数时,若俯视刻度线,则溶液的质量分数将
偏高
偏高
(填“偏低”、“偏高”或“不变”).分析:(1)操作步骤是:计算→称量→溶解→装瓶→贴签→入柜.
(2)只要能改变食盐与水的接触机会就能改变食盐的溶解速率,搅拌、升温都能加快水分子运动速度,也就能加快食盐与水的接触机会,从而加快了食盐的溶解速率.
(3)根据粗盐提纯的步骤分析.
(4)若NaCl末经干燥相当于称量的NaCl减少.
(5)俯视读数,量取的水偏少,则配制的溶液的溶质的质量分数偏高;
(2)只要能改变食盐与水的接触机会就能改变食盐的溶解速率,搅拌、升温都能加快水分子运动速度,也就能加快食盐与水的接触机会,从而加快了食盐的溶解速率.
(3)根据粗盐提纯的步骤分析.
(4)若NaCl末经干燥相当于称量的NaCl减少.
(5)俯视读数,量取的水偏少,则配制的溶液的溶质的质量分数偏高;
解答:解:(1)实验室配制50克溶质质量分数为10%的氯化钠溶液,首先计算配制溶液所需氯化钠和水的质量,再称量所需的氯化钠和量取水,最后进行溶解.故实验室配制50克溶质质量分数为1%的氯化钠溶液的步骤是计算、称量、量取、溶解.
故填:计算;称量;量取;溶解;
(2)据生活经验,影响食盐在水中溶解速率的因素有温度、食盐颗粒大小和搅拌等,搅拌、升温都能加快水分子运动速度,也就能加快食盐与水的接触机会,从而加快了食盐的溶解速率,固体颗粒大小决定了固体与水的接触面积的大小,也能改变溶解速率;
故填:用玻璃棒不断搅拌;加热;将食盐颗粒粉碎.
(3)在粗盐提纯时,首先要将粗盐配成溶液,然后用过滤的方法将泥沙除去,再对滤液进行蒸发操作使晶体逐渐的析出,
故填:溶解;过滤;蒸发
(4)实验中,若NaCl末经干燥,使得称量数据=水分+NaCl,使NaCl实际质量减小,则溶质的质量分数将偏低.
故填:偏低
(5)量取水时俯视凹液面最低处,会使得量取水的体积小于40mL,则所得溶液的溶质质量分数为大于10%;
故填:偏高
故填:计算;称量;量取;溶解;
(2)据生活经验,影响食盐在水中溶解速率的因素有温度、食盐颗粒大小和搅拌等,搅拌、升温都能加快水分子运动速度,也就能加快食盐与水的接触机会,从而加快了食盐的溶解速率,固体颗粒大小决定了固体与水的接触面积的大小,也能改变溶解速率;
故填:用玻璃棒不断搅拌;加热;将食盐颗粒粉碎.
(3)在粗盐提纯时,首先要将粗盐配成溶液,然后用过滤的方法将泥沙除去,再对滤液进行蒸发操作使晶体逐渐的析出,
故填:溶解;过滤;蒸发
(4)实验中,若NaCl末经干燥,使得称量数据=水分+NaCl,使NaCl实际质量减小,则溶质的质量分数将偏低.
故填:偏低
(5)量取水时俯视凹液面最低处,会使得量取水的体积小于40mL,则所得溶液的溶质质量分数为大于10%;
故填:偏高
点评:熟记固体溶解性的影响因素:溶质的性质、溶剂的性质、温度.并知道是如何影响的.

练习册系列答案
相关题目
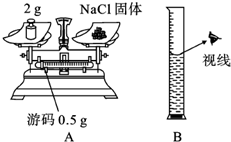 实验室欲配制50g 质量分数为5%的氯化钠溶液.试按下面要求回答问题:
实验室欲配制50g 质量分数为5%的氯化钠溶液.试按下面要求回答问题: