题目内容
【题目】如图是通电分解水的简易装置.据图回答:
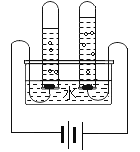
(1)电解水实验:实验前加入少量的氢氧化钠溶液,目的是_____;与电源负极相连的试管内产生的气体是_____,与电源正极相连的试管内产生的气体是_____,负极产生的气体与正极产生的气体的体积比为_____.
(2)电源正极产生的气体应该如何检验____________.
(3)电解水的化学方程式是_____,属于_____反应(填化合或分解).
【答案】增强导电性 氢气 氧气 2:1 将带火星的木条伸入试管中,看带火星的木条能否复燃 2H2O![]() 2H2↑+ O2↑ 分解
2H2↑+ O2↑ 分解
【解析】
(1)纯净的水几乎不导电,为了增强导电性,可加入少量的氢氧化钠溶液;电解水时,正氧负氢,氢二氧一,所以与电源负极相连的试管内产生的气体是氢气,与电源正极相连的试管内产生的气体是氧气,氢气与氧气的体积比为2:1。
(2)电源正极产生的气体是氧气,检验氧气用带火星的木条,氧气能使带火星的木条复燃。(3)水在通电条件下,发生分解反应生成氢气和氧气,由一种物质发生化学反应生成两种或两种以上物质的反应是分解反应。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目