题目内容
【题目】将20g黄铜(由铜、锌组成的合金)样品研磨成粉末,再加入10%的稀硫酸充分反应,所加稀硫酸与生成气体的质量关系如图。请计算:

(1)将黄铜研磨成粉末的目的是__________________.
(2)样品中铜的质量为___________?
(3)图中“?”处应标注的稀硫酸质量应为______________?
【答案】 增大反应物的接触面积,使反应更充分 13.5g 98g
【解析】(1)根据将黄铜研磨成粉末的目的是增大反应物的接触面积,使反应更充分解答;(2)(3)锌和稀硫酸反应生成硫酸锌和氢气,根据氢气的质量计算锌的质量,进一步计算铜的质量和反应的硫酸的质量,从而计算稀硫酸的质量。(1)将黄铜研磨成粉末的目的是增大反应物的接触面积,使反应更充分;
(2)由图可知,反应生成氢气的质量为0.2g。设锌的质量为x,反应的硫酸的质量为y。
Zn+H2SO4=ZnSO4+H2↑
65 98 2
x y 0.2g
![]()
x=6.5g
y=9.8g
样品中铜的质量为20g-6.5g=13.5g
(3)图中“?”处应标注的稀硫酸质量应为9.8g÷10%=98g
答:(2)样品中铜的质量为13.5g;(3)图中“?”处应标注的稀硫酸质量应为98g。

 阅读快车系列答案
阅读快车系列答案【题目】在一次用餐中,同学们对燃料“固体酒精”产生了好奇,于是对其成分进行研究。
【查阅资料】(1)该固体酒精是用酒精、氯化钙和氢氧化钠按一定的质量比混合制成.
(2)氯化钙、氯化钡溶液均呈中性.
【提出问题】(1)酒精中是否含有碳元素?
(2)固体酒精中的氢氧化钠是否变质?
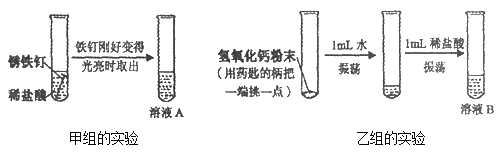
【实验探究】(1)按图实验,发现澄清石灰水变浑浊,可得出酒精中含有碳元素的结论.此结论_____________(选填“合理”或“不合理”).

(2)取少量固体酒精于烧杯中,加足量的水充分溶解后静置,发现烧杯底部有白色沉淀.取沉淀与试管中加稀盐酸,有气泡产生.写出产生沉淀的化学方程式____________.分析实验并结合资料得出氢氧化钠已变质.
(3)为进一步确定氢氧化钠的变质程度,分组探究.
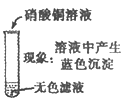
①甲组取烧杯上层清液于两支试管中,按下图探究.
方案 |
|
|
现象 | 溶液变红 | 产生______________ |
结论 | 清液中有氢氧化钠 | 清液中有碳酸钠 |
②乙组认为甲组实验不能证明清液中一定有氢氧化钠,理由是 ____________.他们另取烧杯中上层清液,加足量氯化钡溶液,充分反应后滴加酚酞溶液,酚酞溶液变红.
【实验结论】经讨论一致认为固体酒精中的氢氧化钠部分变质.
【反思交流】乙组实验中加足量氯化钡溶液的目的是 ____________
【拓展应用】要除去部分变质的氢氧化钠溶液中的杂质,可选择适量的____________ .(填序号)
A.Ba(OH)2溶液 B.CaCl2溶液 C.Ca(OH)2溶液